Перейти к:
Исследования реальной клинической практики в онкологии: анализ российских публикаций
https://doi.org/10.37489/2782-3784-myrwd-50
EDN: DIHPQG
Аннотация
Обоснование. Исследования реальной клинической практики — это важный источник знания об онкологических заболеваниях и методах их лечения, что в свою очередь является необходимых инструментом при принятии решений для сотрудников здравоохранения и пациентов. В связи с этим в данной работе был проведён анализ подобных исследований, опубликованных в российской научной литературе.
Цель. Выявить и проанализировать исследования реальной клинической практике в области онкологии.
Материалы и методы. Был проведён систематический обзор и анализ полнотекстовых публикаций в российских рецензируемых медицинских журналах за 2022 и 2023 гг.
Результаты. Было отобрано и проанализировано 119 публикаций. Были определены следующие изучаемые показатели: 1) данные о практике ведения пациентов; 2) выживаемость и другие исходы вне зависимости от лечебных подходов; 3) выживаемость и другие исходы в зависимости от применяемых лечебных подходов; 4) показатели эффективности конкретного лечения; 5) данные о безопасности (токсичности) лечения; 6) клинико-демографические прогностические факторы; 7) определение опухолевых (гистологические, молекулярно-генетические) прогностических факторов; 8) свойства злокачественной опухоли (гистологических, молекулярно-генетических) без определения их прогностического значения; 9) характеристики заболевания (например, сопутствующие заболевания) без определения их прогностического значения. Наиболее частыми изучаемыми показателями были: определение клинико-демографических прогностических факторов — 24 исследования; определение опухолевых прогностических факторов — 36 исследований; определение свойств злокачественной опухоли (гистологические, молекулярно-генетические) без определения их прогностического значения — 38 исследований.
Выводы. Современные исследования реальной клинической практики в онкологии являются важнейшим источником знаний о злокачественных заболеваниях и методах их лечения.
Для цитирования:
Ачикян В.Ф., Курылев А.А., Колбин А.С. Исследования реальной клинической практики в онкологии: анализ российских публикаций. Реальная клиническая практика: данные и доказательства. 2024;4(1):45-65. https://doi.org/10.37489/2782-3784-myrwd-50. EDN: DIHPQG
For citation:
Achikyan V.F., Kurylev A.A., Kolbin A.S. Real-world data studies in oncology: analysis of the Russian publications. Real-World Data & Evidence. 2024;4(1):45-65. (In Russ.) https://doi.org/10.37489/2782-3784-myrwd-50. EDN: DIHPQG
Введение / Introduction
Исследования реальной клинической практики (англ. Real-World Data; RWD) позволяют получить дополнительные важные данные о лекарственном препарате, о применяемых лечебных подходах, что имеет особое значение в онкологии. Как и любой инструмент, они имеют свои ограничения и проблемы, требующие взвешенного подхода при их проведении [1]. Несмотря на то, что на данный момент не существует общепринятого международного подхода в отношении методологии проведения и правового статуса таких исследований, специалисты проводят большую работу собирая, консолидируя и анализируя RWD, которые несомненно несут ценность для медицинского сообщества, регуляторных органов и пациентов. Данные клинических исследований (в том числе неинтервенционных) могут быть применены для принятия клинических или регуляторных решений, с целью улучшение исходов ведения онкологических пациентов. Исследования реальной клинической практики наряду с интервенционными исследованиями являются источником ценнейшей медицинской информации о заболеваниях, практике оказания медицинской помощи, методах лечения, краткосрочных и долгосрочных исходах. Получаемые в ходе этих исследований данные анализируется и используются для принятия как клинических, так и для регуляторных решений [2]. В бурно развивающейся онкологической области также проводится большое количество научных работ, посвящённых ведению пациентов в реальной практике, включая диагностику (инструментальную, лабораторную), маршрутизацию, лечение (лекарственное, хирургическое, лучевое, комбинированное противоопухолевое, поддерживающее), оценку качества жизни, определение прогностических факторов и т. д.
Цель / Objective
Провести систематический обзор и анализ литературы исследований реальной клинической практики в онкологии в России.
Материалы и методы / Materials and methods
Были проанализированы полнотекстовые публикации в рецензируемых медицинских онкологических журналах. Выбирали статьи, посвящённые исследованиям, в которых пациенты получали противоопухолевую, поддерживающую, сопроводительную лекарственную терапию в рамках RWD. Сам термин «данные реальной клинической практики» и связанный с ним термин «доказательства, полученные на основе данных реальной клинической практики» (англ. Real-World Evidence; RWE) закреплён на законодательном уровне в Евразийском экономическом союзе (ЕАЭС) в марте 2022 года [3]. Однако в Российской Федерации определение не имеет пока правового статуса.
В связи с тем, что в подавляющем большинстве случаев в публикациях среди ключевых слов отсутствовали термины «реальная клиническая практика», «данные реальной клинической практики», мы анализировали все публикации в журналах за 2022 и 2023 год, опубликованные в электронном виде на конец января 2024 года.
В данный анализ не включали статьи, посвящённые клиническим случаям или сериям клинических случаев, популяционные эпидемиологические исследования, социологические исследования, метаанализы, исследования на основе математического моделирования, научные проекты, посвящённые разработке новых лечебно-диагностических подходов (клинические исследования, исследования с участием здоровых добровольцев, научные программы валидации новых диагностических процедур и методик, а также опросники пациентов), исследования, которые предусматривали применение лекарственных препаратов не по зарегистрированным показаниям, включая программы раннего доступа, исследования, в которых применялись диагностические процедуры, проведённые с целью получения научной информации. Также в анализ не включались публикации, в которых не описывалось или не подразумевалось лекарственное лечение, например исследования с описанием исходов только хирургического и/или радиологического лечения. Схема отбора публикаций для анализа представлена на рис. 1.

Рис. 1. Алгоритм отбора публикаций
Figure 1. Algorithm for selecting publications
В выбранных публикациях анализировали:
- цель исследования;
- дизайн исследования;
- размер выборки;
- неинтервенционные исследовательские мероприятия (например, оценка выживаемости, определение клинико-демографических факторов риска, молекулярных и/или гистологических характеристик опухоли и др.);
- терапию, назначенную в рамках реальной клинической практики;
- определялись исследуемые показатели.
В ходе анализа полученной информации были определены следующие виды показателей и исходов исследований RWD:
- данные о практике ведения пациентов;
- выживаемость и другие исходы вне зависимости от лечебных подходов;
- выживаемость и другие исходы в зависимости от применяемых лечебных подходов;
- показатели эффективности конкретного лечения;
- данные о безопасности (токсичности) лечения;
- клинико-демографические прогностические факторы;
- определение опухолевых (гистологических, молекулярно-генетических) прогностических факторов;
- свойства злокачественной опухоли (гистологические, молекулярно-генетические) без определения их прогностического значения;
- характеристики заболевания (например, сопутствующие заболевания) без определения их прогностического значения.
Результаты / Results
Всего было выбрано и проанализировано 119 полнотекстовых публикаций 2022 и 2023 гг. из 14 журналов. Список журналов и число статей в каждом из них перечислены в таблице. Исследования были посвящены таким заболеваниям как рак молочной железы, рак яичников, рак пищевода, рак желудка, рак поджелудочной железы, рак толстой и прямой кишки, немелкоклеточный рак лёгкого, хронический лимфолейкоз, множественная миелома, острый лимфобластный лейкоз, меланома, почечно-клеточный рак, рак головы и шеи и др.
Таблица. Специализированные научные онкологические журналы,
публикации из которых вошли в анализ
|
Название журнала |
Число публикаций |
|
Современная онкология |
22 |
|
Вопросы онкологии |
22 |
|
Сибирский онкологический журнал |
18 |
|
Онкология. Журнал им. П. А. Герцена |
15 |
|
Поволжский онкологический вестник |
10 |
|
Успехи молекулярной онкологии |
7 |
|
Российский биотерапевтический журнал |
5 |
|
Злокачественные опухоли |
5 |
|
Российский онкологический журнал |
3 |
|
Онкогинекология |
3 |
|
Южно-Российский онкологический журнал |
3 |
|
Практическая онкология |
3 |
|
Тазовая хирургия и онкология |
2 |
|
Саркомы костей, мягких тканей и опухоли кожи |
1 |
|
Всего |
119 |
Среди всех исследований было 9 регистровых, в которых размер выборки исследования варьировал от 9 до 406 987 человек [4–12]. Показатели и исходы регистровых исследований представлены на рис. 2.
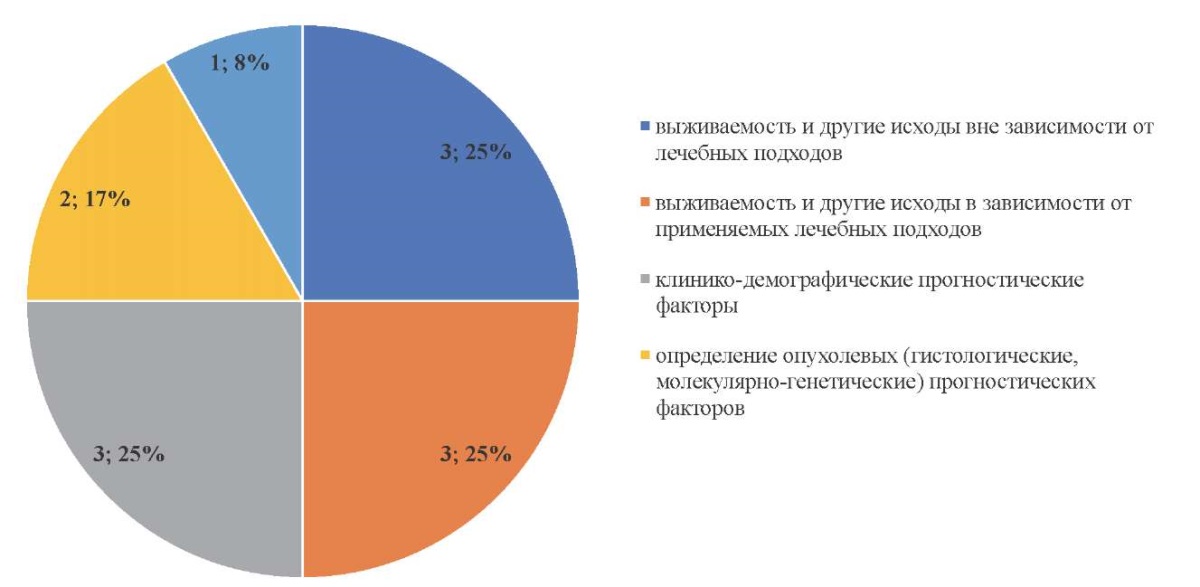
Рис. 2. Показатели и исходы регистровых исследований
Figure 2. Indicators and outcomes of register studies
Остальные 110 публикаций были посвящены нерегистровым исследованиям [13–122]. Размер выборки в них составил от 15 до 1531 человека. Дизайн был ретроспективный (n=70), не ретроспективный (проспективные и одномоментные исследования, n=43), ретроспективно-проспективный (n=6). Подавляющее большинство нерегистровых исследований были одноцентровыми — 105 из 110. Распределение публикаций по показателям и исходам представлено на рис. 3.
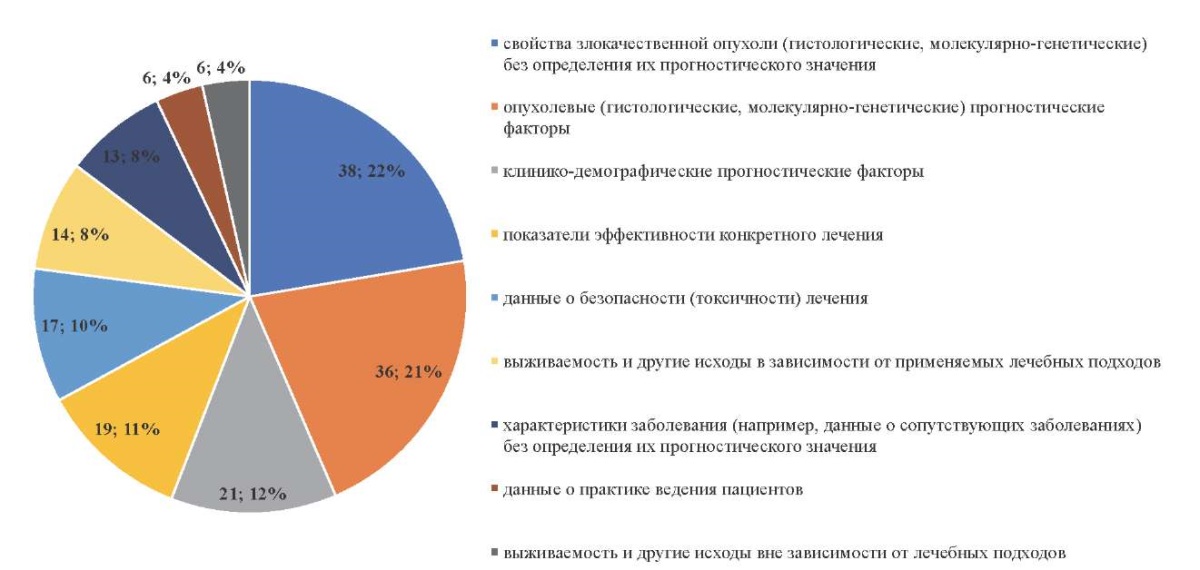
Рис. 3. Показатели и исходы нерегистровых исследований
Figure 3.Indicators and outcomes of non-register studies
Как видно исходя из данных, представленных на рис. 3, около половины нерегистровых исследований составляют работы, посвящённые изучению свойств опухоли и прогностических маркеров.
Анализ публикаций и обсуждение / Analysis of publications and discussion
В соответствии с определёнными показателями и исходами, ниже приведены примеры исследований, вошедших в анализ.
Данные о практике ведения пациентов.В ретроспективном исследовании (n=988) Сапожникова К. В. и соавт. (2023 г.) изучали вопрос влияния профилактики фебрильной нейтропении (ФН) лекарственными препаратами класса гранулоцитарных колониестимулирующих факторов (Г-КСФ) у онкологических пациентов в реальной клинической практике. В данном исследовании была изучена структура встречаемости такого жизнеугрожающего осложнения химиотерапии как ФН, а также практика назначения Г-КСФ. Была выявлена недостаточная частота их назначения у пациентов, получающих противоопухолевое лечение с высоким риском развития ФН. Авторы обратили внимание на недостаточную обеспеченность пациентов первичной профилактикой ФН, следствием чего является развитие тяжёлых осложнений, снижение приверженности химиотерапии и показателей выживаемости [23].
В ретроспективном многоцентровом исследовании Лактионова К. К. и соавт. (2023 г.) были проанализированы истории болезни 514 пациентов в 29 центрах. Целью исследования было определение основных стратегий лечения пациентов с немелкоклеточным раком лёгкого III–IV стадией, проведения независимой оценки эффективности комплекса диагностических мероприятий, оценка эффективность различных лечебных тактик. Было показано, что первую линию лекарственной противоопухолевой терапии получил 361 пациент. Химиотерапия была назначена 333 (92,2 %) пациентам. В 70 % случаев проводилась комбинированная платиносодержащая химиотерапия. Среднее число курсов первой линии химиотерапии составило 4 (от 2 до 6). Объективный эффект составил 32,78 %, стабилизация — 27,78 %, контроль роста опухоли — 60,56 %, прогрессирование — 39,44 %. Иммуноонкологические препараты в первой линии получили 156 пациентов. Таргетные препараты в первой линии получили 25 из 60 пациентов с выявленными активирующими мутациями [68].
Выживаемость и другие исходы вне зависимости от лечебных подходов.В ретроспективном сравнительном исследовании Мурзо В. В. и соавт. (2023 г.) проводилась сравнительная оценка непосредственных и отдалённых результатов химиолучевой терапии у пациентов с плоскоклеточным раком прямой кишки (пРПК, n=15) по сравнению с плоскоклеточным раком анального канала (пРАК, n=15), получавших сходную химиолучевую терапию. Было показано, что общая и безрецидивная выживаемость не были достоверно снижены у пациентов с пРПК относительно пациентов с пРАК, однако для пРПК была характерна более низкая частота полных клинических ответов на проводимое лечение [51].
В работе Каганова О. И. и соавт. (2022 г.) описываются результаты лечения пациентов с раком поджелудочной железы, а также собираются данные о практике оказания медицинской помощи за последние 5 лет. Представлены данные 213 пациентов, получивших хирургическое лечение, включая 12 пациентов, получивших неоадъювантную химиотерапию. Описаны данные о первичной диагностике и верификации диагноза, оказанной специализированной хирургической помощи и химиотерапии, распределении по стадиям, клинико-демографических характеристиках пациентов, гистологии опухоли, послеоперационных осложнениях. Средний возраст больных составил 62,2 года, общая выживаемость во всей группе была 20 месяцев. Наиболее благоприятный прогноз в группе больных с IA стадией, где 1-летняя выживаемость составляет 50,98 %, а 5-летняя выживаемость — 17,64 % [109].
Выживаемость и другие исходы в зависимости от применяемых лечебных подходов.В ретроспективном регистровом исследовании Тонеева Е. А. и соавт. (2023 г.) с участием 141 пациента с раком пищевода сравнивались показатели выживаемости при применении двух лечебных подходов: химиолучевой терапии и химиолучевой терапии с последующей радикальной операцией. По данным исследования, общая 5-летняя выживаемость в группе не оперированных и оперированных больных составила 24,0 и 27,0 % (p=0,020), 5-летняя безрецидивная выживаемость — 23,0 и 25,0 % (p=0,018), а трёхлетняя выживаемость составила 21 и 45 %, соответственно (p=0,050) [10].
В публикации Хатькова И. Е. и соавт. (2023 г.) представлены результаты ретроспективного исследования, в котором ретроспективно сравнивали выживаемость пациентов с первично операбельным раком поджелудочной железы в зависимости того, какой режим химиотерапии применялся: неоадъювантный (n=45) или адъювантный (n=153). Медиана времени наблюдения составила 41,7 мес. (либо от начала неоадъювантной химиотерапии, либо от даты хирургического вмешательства). Оценивалась безрецидивная и общая выживаемость. Было показано, что отделённые результаты в двух группах практически не отличаются друг от друга [19].
Показатели эффективности конкретного лечения. В сравнительном ретроспективном исследовании Ходырева С. А. и соавт. (2023 г.) проводилась оценка эффективности гидроксиэтилдиметилдигидропиримидина в отношение качества жизни, системных воспалительных и локальных хирургических проявлений у пациенток, перенёсших реконструктивно-восстановительные операции (РВО) после мастэктомии. 10 из 75 пациенток проводили РВО отсрочено. Сравнение проводили с пациентками, которым гидроксиэтилдиметилдигидропиримидин не назначался в раннем послеоперационном периоде. В исследовании было показано, что назначение данного лечения ассоциировалось со значительным уменьшением выраженности воспалительной реакции в операционной ране, уменьшением длительности лимфореи и сроков удаления улавливающих дренажей, более благоприятными показателями качества жизни в периоде реабилитации [20].
В когортном исследовании Меньшикова К. В. и соавт. (2022 г.) изучались результаты применения кабозантиниба с распространённым почечно-клеточным раком. 48 пациентов (16,2 %) получали лечение в монорежиме и 3 пациента (1 %) — в комбинации с ниволумабом. Объективный ответ был задокументирован у 78,9 % пациентов после трёх курсов лечения. Наряду с тем, что лечение показало удовлетворительный профиль переносимости, авторы отметили, что результаты применения препарата в реальной клинической практике соответствуют показателям, полученным в клинических исследованиях [90].
Данные о безопасности (токсичности) лечения. Многоцентровое проспективное исследование ROSCARCC было посвящено изучению безопасности и анализу влияния токсичности монотерапии кабозантинибом на эффективность лечения пациентов с диссеминированным почечно-клеточным раком. В 16 центрах последовательно было включено 92 пациента, которым был назначен кабозантиниб, в соответствии с инструкцией по применению. Нежелательные явления были зарегистрированы у 88,0 % пациентов, нежелательные явления 3–4-й степени тяжести развились в 32,6 % случаев. У пациентов с артериальной гипертензией, развившейся на фоне лечения, отмечено достоверное увеличение выживаемости без прогрессирования (ОР 2,5; 95 % ДИ 1,0–5,9; p=0,046) и общей выживаемости (ОР 3,0; 95 % ДИ 1,2–8,3; p=0,025) [21].
В ретроспективное исследование Дегтяревой Е. А. и соавт. (2022 г.) были включены пациенты (n=178), получившие иммунотерапию по поводу солидных злокачественных опухолей. Иммуноопосредованные нежелательные явления развились у 32,6 %, самыми частыми из которых стали дисфункция печени (11,2 %) и щитовидной железы (10,1 %). Осложнения 3 степени тяжести и выше наблюдались в 15,7 % случаев. Авторы сделали вывод, что в проанализированной выборке российских пациентов, получавших терапию ингибиторами PD-1 и PD–L1, зафиксирована меньшая частота осложнений [44].
Клинико-демографические прогностические факторы. В исследовании Громова Д. Д. и соавт. (2023 г.) по материалам Архангельского областного канцер-регистра определялись клинические, морфологические, демографические характеристики в качестве предикторов 1-летней и 5-летней выживаемости при раке яичников. Было проанализировано 2703 клинических случая. На опухолеспецифическую выживаемость определялось влияние следующих факторов: возраст, место проживания, временной период получения лечения, наличие сведений о специальном противоопухолевом лечении. Авторы отметили, что помимо известных клинических факторов прогноза, стадии и гистологического варианта рака яичников, сильное неблагоприятное влияние на исход оказывают пожилой возраст и факт проживания в удалённых районах области [6].
В регистровое многоцентровое (7 центров) ретроспективное исследование Тимофеева И. В. и соавт. (2023 г.) было включено 175 пациентов с раком пищевода. Проводилась оценка влияния на прогноз пола, возраста, гистологического подтипа, системной лекарственной терапии при метастатическом заболевании. Продолжительность жизни пациентов, получивших хотя бы одну линию терапии (медиана 11,0 мес.; 95 % ДИ 7,9–14,1), была достоверно дольше, чем пациентов, не получавших лечение (2,4 мес.; 95 % ДИ 1,6–3,2; p <0,0001). В многофакторном анализе было выявлено 2 независимых фактора, влияющих на общую выживаемость — наличие системной и/или лучевой терапии (все p <0,0001) и ответ на химиотерапию (p <0,001) [8].
Определение опухолевых (гистологические, молекулярно-генетические) прогностических факторов. Публикация Стукань А. И. и соавт. (2023 г.), посвящённая изучению влияния уровня экспрессии рецепторов стероидных гормонов и HER2 в первичной опухоли и метастатическом очаге на риск прогрессирования на монотерапии эрибулином при раке молочной железы (n=61). Было показано, что риск прогрессирования возрастал при комбинации следующих показателей: уровень экспрессии эстрогеновых рецепторов (ЭР) в первичной опухоли > 90 %; уровень экспрессии ЭР в метастазе > 50 %; уровень экспрессии прогестероновых рецепторов (ПР) в метастазе > 20 %; негативный и низкий уровень экспрессии HER2 в метастазе (0, 1+) (AUC = 0,614 ± 0,092 (95 % ДИ 0,510–0,719) р = 0,0289) [36].
В публикации Завьяловой М. В. и соавт. (2022 г.) описаны результаты исследования с участием 72 пациенток с раком молочной железы, которым после трепанобипсии и подтверждения диагноза получили хирургическое лечение и неоадъювантное, адъювантное химиолучевое лечение по показаниям. В клетках первичной опухоли оценивалась экспрессия группы маркеров интегринов: CD61 (Integrin beta 3), CD104 (Integrin beta 4), CD51 (Integrin alpha-V). Также при исследовании операционного материала устанавливался факт наличия или отсутствия метастазов в регионарных лимфоузлах: у 50 пациенток были обнаружены метастазы, а у 22 — не были. При сравнении экспрессии интегринов в этих двух подгруппах пациенток, было показано, что экспрессия CD104 в клетках первичной опухоли имеет выраженную ассоциацию с распространённым лимфогенным метастазированием [64].
Свойства злокачественной опухоли (гистологических, молекулярно-генетических) без определения их прогностического значения. В публикации Соколовой Т. Н. и соавт. (2022 г.) представлены результаты исследования, в рамках которого в образцах опухолевой ткани 694 пациенток с HR+ HER2- первично метастатическим или рецидивирующим рака молочной железы, получавших любую линию противоопухолевой терапии в лечебно-профилактических учреждениях Российской Федерации, были проанализированы экзоны 7, 9 и 20 гена PIK3CA. Использовался метод ПЦР. Мутации выявлены в 32 % случаях. На три наиболее частые миссенс-замены в гене PIK3CA (p. E542K, p. E545K и p. H1047R) пришлось 86 % мутаций. Также были обнаружены ассоциации мутаций с люминальным А подтипом, низким индексом пролиферации, малым размером первичной опухоли, отсутствием признаков наследственного рака [29].
В рамках исследования Журман В. Н. (2023 г.) проведено иммуногистохимическое исследование опухолевого материала у 74 пациенток с серозным раком яичников, получавших лечение в ГБУЗ «Приморский краевой онкологический диспансер». Для определения антигенов в образцах использовали моноклональные антитела: CD3, CD4, CD8, CD11b, CD14 и CD16. Был сделан ряд наблюдений. Например, в составе иммунных клеток микроокружения наибольшее количество клеток, при всех стадиях (I–IV) онкологического процесса, представлено макрофагами (СD11b+, CD14+), на втором месте по количеству клеток были СD3+ лимфоциты. С увеличением стадии заболевания число макрофагов (СD11b+, CD14+) и лимфоцитов (СD3+, CD16+) уменьшалось независимо от степени дифференцировки [85].
Характеристики заболевания (например, сопутствующие заболевания) без определения их прогностического значения. В публикации Колтаковой А. Д. и соавт. (2023 г.) представлены результаты исследования, в котором изучалась структура скелетно-мышечной патологии у пациентов, находящихся в процессе лекарственной терапии по поводу злокачественного новообразования. Ревматологом была обследована выборка из 140 пациентов, проходящих лечение в дневном стационаре отдела лекарственного лечения опухолей МНИОИ имени П. А. Герцена. У 81 % пациентов присутствовали различные скелетно-мышечные проявления, которые включали в себя боль в суставах у 59,3 % пациентов, у 10 % — в мышцах, у 10 % — в костях, у 5 % — скованность в суставах более 30 мин по утрам, у 13,6 % — припухание в области суставов, у 27 % — боль в спине. При этом 39,3 % пациентов скелетно-мышечная патология была ассоциирована с проводимой лекарственной противоопухолевой терапией [37].
В ретроспективном исследовании Манихаса Г. М. и соавт. (2022 г.) были проанализированы медицинские данные 98 пациентов с раком лёгкого и ВИЧ-инфекцией, получавших антиретровирусную терапию. В исследуемой популяции преобладали пациенты молодого и среднего возрастов, пациентов пожилого возраста (60–74 лет) было 11,2 % (p < 0,001), что соответствует общемировым данным о более раннем возникновении рака лёгкого у ВИЧ-инфицированных. Как и в общей популяции, среди гистологических типов злокачественных новообразований чаще встречалась аденокарцинома лёгкого (p <0,001). Не выявлено статической значимости между высокой вирусной нагрузкой и раком лёгкого [111].
Выводы / Conclusions
Современные исследования RWD/RWE затрагивают самые разные аспекты онкологической области: лабораторная и инструментальная диагностика злокачественных опухолей (в том числе редких) и сопутствующих заболеваний, маршрутизация пациентов, противоопухолевое лечение (химотерапия, таргетная терапия, иммунотерапия, лучевая терапия, хирургия, комбинированное лечение), сопроводительное лечение, краткосрочное и долгосрочное наблюдение пациентов, оценка биологических свойств опухоли. Благодаря активному внедрению в современную научную повестку исследования реальной клинической практики являются исключительно важным источником данных, которые необходимы для изучения практики ведения пациентов, безопасности противоопухолевой терапии, эффективности того или иного подхода к лечению пациентов, а также выявления значимых прогностических факторов, клинико-демографических и опухолевых. Полученные таким образом данные могут быть использованы для принятия клинических и регуляторных решений, направленных на совершенствование оказания медицинской помощи. Анализ научной литературы, проведённый в рамках данной работы, показал, что большая часть современных исследований RWD/RWE в области онкологии посвящена вопросам изучения свойств злокачественных опухолей и опухолевых прогностических факторов.
ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ
Конфликт интересов.
Авторы декларирует отсутствие конфликта интересов.
Финансирование.
Исследование не имело спонсорской поддержки.
Участие авторов. Все соавторы подтверждают окончательный вариант статьи, ответственность за целостность всех частей статьи. Ачикян В. Ф. — концепция, дизайн исследования, сбор и обработка материала, написание текста, составление списка литературы; Курылев А. А. — редактирование; Колбин А. С. — концепция, дизайн исследования, редактирование.
ADDITIONAL INFORMATION
Conflict of interests.
The author declares no conflict of interest.
Financing.
The study had no sponsorship.
Participation of authors. All authors are responsible for the integrity of all parts of the manuscript and approval of its final version. Achikyan VF — research concept and design, collection and processing, writing the text, compilation of the list of literature; Kurylev AA — editing; Kolbin AS — research concept and design, editing.
Список литературы
1. Журавков А.А., Моисеенко Ф.В., Колбин А.С., Моисеенко В.М. Исследования реальной клинической практики в онкологии: тренд или необходимость? Практическая онкология. 2023;24(1):59-69. https://www.doi.org/10.31917/2401059.
2. Исследования реальной клинической практики. Обновлённые рекомендации 2023 года. / под общей редакцией Колбина А. С. — М. : Издательство ОКИ, 2023. — 222 с. : ил. ISBN 978-5-907715-17-2 https://izdat-oki.ru/issledovaniya-realnoj-klinicheskoj-praktikiobnovlyonnyerekomendacii-2023-goda
3. Решение Совета Евразийской экономической комиссии от 17 марта 2022 г. № 36 «О внесении изменений в Правила регистрации и экспертизы лекарственных средств для медицинского применения».
4. Фридман М.В., Левин Л.Ф., Леонова Т.А., и др. Клинико-морфологическая характеристика пациентов с метастазами папиллярного рака щитовидной железы в головном мозге. Вопросы онкологии. 2023;69(6):1065−1072. doi: 10.37469/0507-3758-2023-69-61065-1072.
5. Агаева А.В., Громов Д.Д., Чемакина О.В., и др. Влияние суррогатных молекулярно-биологических подтипов рака молочной железы на выживаемость: углубленный эпидемиологический анализ по данным Архангельского областного регистра рака. Вопросы онкологии. 2023;69(4):639-647. doi: 10.37469/0507-3758-2023-69-4-639-647.
6. Громов Д.Д., Чемакина, О.В., Светлакова А.В., и др. Предикторы выживаемости при раке яичников: популяционное исследование по данным областного регистра рака. Вопросы онкологии. 2023;69(3):406–414. doi: 10.37469/0507-3758-2023-69-3-406-414.
7. Мерабишвили В.М., Беляев А.М. Состояние онкологической помощи в России: динамика пятилетней выживаемости больных злокачественными новообразованиями и её ранговое распределение по всем локализациям опухолей. Популяционное исследование на уровне Северо-Западного федерального округа. Вопросы онкологии. 2023;69(2):227–237. doi: 10.37469/0507-3758-2023-69-2227-237.
8. Тимофеев И.В., Зуков Р.А., Петкау В.В., и др. Продолжительность жизни пациентов с метастатическим раком пищевода: российское многоцентровое регистровое исследование. Voprosy Onkologii. 2023;69(1):82-88. doi: 10.37469/0507-3758-2023-69-1-82-88.
9. Жерко И.Ю., Науменко Л.В., Жиляева Е.П., и др. Результаты лечения пациентов с метастатической увеальной меланомой: ретроспективное моноцентровое исследование. Вопросы онкологии. 2022;68(2):224–231. https://doi.org/10.37469/0507-3758-2022-68-2-224-231.
10. Тонеев Е.А., Пикин О.В., Деньгина Н.В., и др. Результаты комбинированного и химиолучевого лечения больных раком грудного отдела пищевода по данным регионального онкологического центра. Сибирский онкологический журнал. 2023;22(5):84-95. https://doi.org/10.21294/1814-4861-2023-22-5-84-95.
11. Петкау В.В., Бессонова Е.Н., Бредер В.В., и др. Влияние мультидисциплинарного подхода и маршрутизации пациентов на результаты лечения больных гепатоцеллюлярным раком. Злокачественные опухоли. 2023;13(2):5-11. https://doi.org/10.18027/2224-5057-2023-13-2-1.
12. Петкау В.В., Е.Н. Бессонова Е.Н., Бредер В.В., и др. Общая выживаемость пациентов с гепатоцеллюлярной карциномой различной этиологии. Практическая онкология. 2023;24(1):7079. https://www.doi.org/10.31917/2401071.
13. Лядов В.К., Федоринов Д.С., Лядова М.А., и др. Саркопения при раке толстой кишки: клинико-рентгенологические корреляции. Современная онкология. 2023;25(3):278-282. doi: 10.26442/18151434.2023.3.202447.
14. Лядова М.А., Федоринов Д.С., Кузьмина Е.С., и др. Опыт применения комбинации тиксагевимаб + цилгавимаб с целью доконтактной профилактики COVID-19 у онкологических пациентов. Современная онкология. 2023;25(3):392-396. doi: 10.26442/18151434.2023.3.202456.
15. Завьялова М.В., Кузнецов Г.А., Григорьева Е.С., и др. Связь интегринового профиля первичной опухоли с метастазированием в регионарные лимфоузлы при раке молочной железы. Современная онкология. 2023;25(3):330-335. doi: 10.26442/18151434.2023.3.202411.
16. Саевец В.В., Шаманова А.Ю. Оценка клинического и экономического преимущества парентерального введения железа карбоксимальтозата у пациенток с онкогинекологической патологией. Современная онкология. 2023;25(3):373-377. doi: 10.26442/18151434.2023.3.202442.
17. Снеговой А.В., Кононенко И.Б., Сорокина И.В., и др. Частота встречаемости схем с высоким риском развития фебрильной нейтропении и частота развития дозолимитирующей нейтропении среди пациентов, получающих цитотоксическую терапию по поводу злокачественных новообразований: результаты исследования FLAME. Современная онкология. 2023;25(3):378-384. doi: 10.26442/18151434.2023.3.202452.
18. Журман В.Н. Характеристика рецепторного фенотипа опухоль-ассоциированных иммунных клеток эпителиально-мезенхимального микроокружения рака яичников. Современная онкология. 2023;25(1):99-103. doi: 10.26442/18151434.2023.1.202076.
19. Хатьков И.Е., Семенов Н.Н., Израилов Р.Е., и др. Роль неоадъювантной химиотерапии у больных первично-резектабельным раком поджелудочной железы. Современная онкология. 2023;25(2):236-240. doi: 10.26442/18151434.2023.2.202295.
20. Ходырев С.А., Шабаев Р.М., Колядина И.В., и др. Гидроксиэтилдиметилдигидропиримидин как препарат выбора для профилактики парапротезных сером в реконструктивной хирургии молочных желез. Современная онкология. 2023;25(2):214-220. doi: 10.26442/18151434.2023.2.202305.
21. Волкова М.И., Калпинский А.С., Меньшиков К.В., и др. Безопасность и токсичность монотерапии кабозантинибом у пациентов с распространенным почечно-клеточным раком: Российское многоцентровое наблюдательное исследование. Современная онкология. 2023;25(2):221-228. doi: 10.26442/18151434.2023.2.202262.
22. Чулкова С.В., Шолохова Е.Н., Поддубная И.В., и др. Взаимосвязь молекул главного комплекса гистосовместимости HLA-I и II классов с клинико-морфологическими признаками рака молочной железы. Современная онкология. 2023;25(2):208-213. doi: 10.26442/18151434.2023.2.202082.
23. Сапожников К.В., Сорокина И.В., Гусев А.В., и др. Профилактика фебрильной нейтропении у онкологических пациентов: данные реальной клинической практики. Современная онкология. 2023;25(1):115-122. doi: 10.26442/18 151434.2023.1.202138.
24. Турупаев К.А., Будурова М.Д., Филиппова М.Г., и др. Молекулярно-генетический ландшафт десмоидного фиброматоза абдоминальной и забрюшинной локализации. Ретроспективное исследование. Современная онкология. 2023;25(1):104-110. doi: 10.26442/18151434.2023.1.202016.
25. Журман В.Н. Клиническая значимость патологоанатомического типа опухоли при распространенных формах рака яичников. Современная онкология. 2023;25(2):241-243. doi: 10.26442/18151434.2023.2.202091.
26. Голубенко Е.О., Савельева М.И., Поддубная И.В., Коренная В.В. Клинические факторы риска гиперпластических процессов эндометрия на терапии тамоксифеном рака молочной железы. Результаты ретроспективного популяционного исследования. Современная онкология. 2023;25(1):63-67. doi: 10.26442/18151434.2023.1.202117.
27. Нестерова Е.С., Сайдуллаева А.Ф., Шерстнев Д.Г., и др. Эффективность и безопасность применения препарата эмпэгфилграстим (Экстимия®, БИОКАД) у пациентов с лимфопролиферативными заболеваниями, получающих цитотоксическую терапию: результаты второго промежуточного анализа многоцентрового ретроспективно-проспективного наблюдательного пострегистрационного исследования LEGERITY. Современная онкология. 2022;24(1):80-88. doi: 10.26442/18151434.2022.1.201493.
28. Волконский М.В., Жихорев Р.С., Макаркина Т.А., и др. Собственный опыт применения ленватиниба у пациентов с распространенным гепатоцеллюлярным раком в условиях реальной клинической практики на базе ГБУЗ «Московская городская онкологическая больница №62». Современная онкология. 2022;24(1):106-109. doi: 10.26442/18151434.2022.1.201477.
29. Соколова Т.Н., Соловьева Т.И., Алексахина С.Н., и др. Клинико-морфологические особенности опухолей молочной железы с мутациями PIK3CA у российских больных: наблюдательное исследование. Современная онкология. 2022;24(1):12-23. doi: 10.26442/8151434.2022.1.201435.
30. Султанбаев А.В., Меньшиков К.В., Мусин Ш.И., и др. Опыт применения олапариба в лечении BRCA-ассоциированных опухолей в реальной клинической практике. Олапариб в режиме Re-Challenge. Наблюдательное исследование. Современная онкология. 2022;24(2):221-225. doi: 10.26442/18151434.2022.2.201550.
31. Чулкова С.В., Шолохова Е.Н., Поддубная И.В., и др. Анализ взаимосвязи трансферринового рецептора 1 (TfR1) с клинико-морфологическими и иммунофенотипическими характеристиками рака молочной железы. Современная онкология. 2022;24(3):355-360. doi: 10.26442/18151434.2022.3.201821.
32. Орлова К.В., Федянин М.Ю., Симаненков К.Э., и др. Эффективность 1-й линии терапии пролголимабом у больных метастатической меланомой в реальной клинической практике: промежуточные результаты наблюдательного исследования FORA «FOrteca Real practice Assessment». Современная онкология. 2022;24(4):413-425. doi: 10.26442/18151434.2022.4.202035.
33. Стилиди И.С., Егенов О.А., Неред С.Н., и др. Рецидив рака яичников с поражением лимфатических узлов: хирургия или химиотерапия? Современная онкология. 2022;24(2):170-176. doi: 10.26442/18151434.2022.2.201692.
34. Гречухина К.С., Чеботарева Н.В., Жукова Г., и др. NGAL и KIM-1 — ранние мочевые биомаркеры нефротоксичности, опосредованной цисплатином: обсервационное исследование. Современная онкология. 2022;24(1):119-124. doi: 10.26442/18151434.2022.1.201285.
35. Загидуллина А.А., Гордеев С.С., Мамедли З.З. Эффективность применения адъювантной химиотерапии у пациентов с перстневидноклеточным раком толстой кишки: ретроспективное исследование. Вопросы онкологии. 2023;69(5):871−875. doi: 10.37469/0507-3758-2023-69-5-871-875.
36. Стукань А.И., Мурашко Р.А., Кутукова С.И., и др. Влияние различий уровня экспрессии рецепторов стероидных гормонов и экспрессии HER2 в первичной опухоли и метастатическом очаге на эффективность монохимиотерапии эрибулином при диссеминированном раке молочной железы. Вопросы онкологии. 2023; 69(4):699–707. doi: 10.37469/0507-3758-2023-69-4699-707.
37. Колтакова А.Д., Лила А.М., Феденко А.А. Спектр скелетно-мышечной патологии у онкологических пациентов. Вопросы онкологии. 2023;69(3):508–515. doi: 10.37469/0507-3758-2023-69-3-508-515.
38. Сунь Х., Неред С.Н., Трякин А.А., и др. Неоадъювантная химиоиммунотерапия у пациентов раком желудка с микросателлитной нестабильностью. Вопросы онкологии. 2023;69(2): 275–284. doi: 10.37469/0507-37582023-69-2-275-284.
39. Холопов Д.В., Вязовая А.А., Лялина Л.В., и др. Вирус папилломы человека при злокачественных новообразованиях различных локализаций. Вопросы онкологии. 2023;69(1):89-94. doi: 10.37469/05073758-2023-69-1-89-94.
40. Соколенко А.П., Иванцов А.О., Городнова Т.В., и др. Иммунное микроокружение в серозных карциномах яичника высокой степени злокачественности: ассоциация с молекулярными характеристиками и ответ на стандартную неоадъювантную терапию. Вопросы онкологии. 2023;69(1):74-81. doi: 10.37469/05073758-2023-69-1-74-81.
41. Минниахметов И.Р., Кагирова Э.М., Машков О.И., Хусаинова Р.И. Поиск патогенных изменений в генах BRCA1/2 с использованием технологии массового параллельного секвенирования у пациентов с раком молочной железы и яичников из Республики Башкортостан. Вопросы онкологии. 2022;68(1):48–54. doi: 10.37469/0507-3758-2022-68-1-48-54.
42. Стогова Н.А. Клинико-морфологические аспекты сочетания туберкулёза и рака лёгких. Вопросы онкологии. 2022;68(1):75–79. doi: 10.37469/0507-3758-2022-68-1-75-79.
43. Спирина Л.В., Тарасова А.С., Добродеев А.Ю., и др. Молекулярные маркеры развития колоректального рака, связь с объективным ответом опухоли на лечение. Вопросы онкологии. 2022;68(1):85–90. doi: 10.37469/0507-3758-2022-68-1-85-90.
44. Дегтярёва Е.А., Проценко С.А., Иевлева А.Г., Имянитов Е.Н. Частота развития иммуноопосредованных нежелательных явлений на фоне анти-PD-1/PD-L1 терапии в реальной клинической практике. Вопросы онкологии. 2022;68(2):188–199. doi: 10.37469/0507-3758-2022-68-2-188-199.
45. Топузов Э.Э., Орлова Р.В., Аршба Э.А., Скворцов В.А. Влияет ли суммарный размер опухоли при мультифокальном /мультицентричном раке молочной железы на выживаемость? Вопросы онкологии. 2022;68(3):333–341. doi: 10.37469/0507-3758-2022-68-3-333-341.
46. Демешко П.Д., Каленик О.А., Поддубный К.В., Гиземова О.А. Прогностическое значение метаболического объема опухоли по данным 18-ФДГ-ПЭТ/КТ у пациентов с впервые выявленной диффузной В-крупноклеточной лимфомой. Вопросы онкологии. 2022;68(4):464–472. doi: 10.37469/0507-3758-2022-68-4-464-472.
47. Сидибе Н., Солодкий В.А., Сотников В.М. Общая выживаемость больных нодальными неходжкинскими лимфомами брюшной полости и таза после химиолучевого лечения и химиотерапии. Вопросы онкологии. 2022;68(4):498–506. doi: 10.37469/0507-3758-2022-68-4-498-506.
48. Югай В., Никулин М., Козлов Н., Мазуренко Н., и др. Клинико-морфологические характеристики пациентов с гастроинтестинальной стромальной опухолью с дефицитом сукцинатдегидрогеназы. Вопросы онкологии. 2022;68(5):614–621. doi: 10.37469/0507-3758-2022-68-5614-621.
49. Омарова Д.Ф., Зикиряходжаев А.Д., Усов Ф.Н., и др. Онкологическая безопасность онкопластических резекций у больных раком молочной железы. Вопросы онкологии. 2022;68(6):752–757. doi: 10.37469/0507-3758-2022-68-6-752-757.
50. Попова М.О., Чекалов А.М., Цыганков И.В., и др. Лимфома Беркитта у пациентов с ВИЧ-инфекцией: результаты российского многоцентрового исследования. Вопросы онкологии. 2022;68(6):786–796. doi: 10.37469/0507-3758-2022-68-6-786-796.
51. Мурзо В.В., Гордеев С.С., Мышляков В.С., Мамедли З.З. Сравнительная эффективность химиолучевой терапии при плоскоклеточном раке прямой кишки и анального канала: исследование с псевдорандомизацией. Сибирский онкологический журнал. 2023;22(4):1421. doi: 10.21294/18144861-2023-22-4-14-21.
52. Кузьмина Е.С., Федянин М.Ю., Решетов И.В., и др. Сравнение эффективности и безопасности терапии регорафенибом и реинтродукции химиотерапии при метастатическом раке толстой кишки — результаты ретроспективного многоцентрового исследования. Сибирский онкологический журнал. 2023;22(4):34-43. doi: 10.21294/1814-4861-2023-22-4-34-43.
53. Сергеева Н.С., Кармакова Т.А., Савчина В.В., и др. Динамика уровня маркера острого повреждения почек KIM-1 в моче онкологических больных, получающих химиотерапию с цисплатином. Сибирский онкологический журнал. 2023;22(4):44-54. doi: 10.21294/1814-4861-2023-22-4-44-54.
54. Юдин Д.И., Лактионов К.К., Саранцева К.А., и др. Клиническое значение легочного иммунного прогностического индекса и его модификации у пациентов с метастатическим НМРЛ, получающих иммунотерапию. Сибирский онкологический журнал. 2023;22(2):5664. doi: 10.21294/1814-4861-2023-22-2-56-64.
55. Журман В.Н., Нечушкина В.М. Опыт применения ингибитора поли (АДФ-рибозо) полимеразы олапариба в поддерживающей терапии BRCA-ассоциированного рака яичников. Сибирский онкологический журнал. 2023;22(1):35-42. doi: 10.21294/1814-4861-202322-1-35-42.
56. Алифанов В.В., Таширева Л.А., Завьялова М.В., Перельмутер В.М. Особенности экспрессии белка LIMCH1, связанные с лимфогенным метастазированием при раке молочной железы. Сибирский онкологический журнал. 2023;22(1):74-81. doi: 10.21294/18144861-2023-22-1-74-81.
57. Кит О.И., Франциянц Е.М., Кательницкая О.В. Риск венозных тромбоэмболических осложнений у больных злокачественными новообразованиями поджелудочной железы. Сибирский онкологический журнал. 2022;21(3):2432. doi: 10.21294/18144861-2022-21-3-24-32.
58. Кнеев А.Ю., Школьник М.И., Богомолов О.А., Жаринов Г.М. Плотность простат-специфического антигена как прогностический фактор у больных раком предстательной железы, перенесших комбинированное гормонолучевое лечение. Сибирский онкологический журнал. 2022;21(3):12-23. doi: 10.21294/18144861-2022-21-3-12-23.
59. Кутилин Д.С., Кит О.И. Зависимость выживаемости и метастазирования у больных колоректальным раком от транскрипционной активности РТ-генов. Сибирский онкологический журнал. 2022;21(1):37-46. doi: 10.21294/1814-4861-2022-21-1-37-46.
60. Телышева Е.Н., Шайхаев Е.Г., Снигирева Г.П. Мутационный профиль КRAS-позитивного колоректального рака. Сибирский онкологический журнал. 2022;21(1):47-56.
61. Коваленко Н.В., Жаворонкова В.В., Иванов А.И., и др. Рак желудка у пациентов моложе и старше 50 лет: характеристики опухолевого процесса, анализ выживаемости. Сибирский онкологический журнал. 2022;21(2):24-37. doi: 10.21294/1814-4861-2022-21-2-24-37.
62. Потемин С.Н., Уваров И.Б., Потемин Д.С. Интраоперационная радиотерапия фотонной радиохирургической системой в лечении местнораспространенного рака прямой кишки. Сибирский онкологический журнал. 2022;21(1):20-28. doi: 10.21294/1814-4861-2022-21-1-20-28.
63. Тихомирова М.В., Бармин В.В., Топчу Ю.А., и др. Экспрессия поддерживающего белка NEDD9 как негативный прогностический маркер при немелкоклеточном раке легкого (НМРЛ). Сибирский онкологический журнал. 2022;21(4):47-55. doi: 10.21294/1814-4861-2022-21-4-47-55.
64. Завьялова М.В., Лоос Д.М., Письменный Д.С., и др. Особенности лимфогенного метастазирования в зависимости от внутриопухолевой гетерогенности немелкоклеточного рака легких у пациентов с разными морфологическими изменениями бронхиального эпителия. Сибирский онкологический журнал. 2022;21(5):69-81. doi: 10.21294/1814-4861-2022-21-5-69-81.
65. Цыганов М.М., Ибрагимова М.К., Гарбуков Е.Ю., и др. Предиктивная и прогностическая значимость явления потери гетерозиготности в генах ABC-транспортеров в опухоли молочной железы. Сибирский онкологический журнал. 2022;21(5):34-43. doi: 10.21294/1814-4861-2022-215-34-43.
66. Бузенкова А.В., Таширева Л.А., Завьялова М.В., Перельмутер В.М. Особенности клеточного состава опухолевой ниши инвазивной протоковой карциномы неспецифического типа молочной железы. Сибирский онкологический журнал. 2022;21(5):59-68. doi: 10.21294/1814-4861-2022-21-5-59-68.
67. Данилко К.В., Еникеева К.И., Кабиров И.Р., и др. Морфологическая гетерогенность внутриопухолевых макрофагов в опухоли предстательной железы. Сибирский онкологический журнал. 2022;21(6):81-90. doi: 10.21294/18144861-2022-21-6-81-90.
68. Лактионов К.К., Реутова Е.В., Горохов А.Е., и др. Подходы к диагностике и лечению больных немелкоклеточным раком легкого III—IV стадии в России. Предварительные результаты проспективного многоцентрового неинтервенционного наблюдательного исследования КАРЛ. Онкология. Журнал им. П.А. Герцена. 2023;12(6):33-37. doi: 10.17116/onkolog20231206133.
69. Чугуев А.С., Кобылецкая Т.М., Беликова А.А., и др. Предикторы первичного прогрессирования при глиобластоме. Онкология. Журнал им. П.А. Герцена. 2023;12(5):13-19. doi: 10.17116/onkolog20231205113.
70. Фатеева А.В., Зуков Р.А., Зюзюкина А.В., и др. Поиск предикторов эффективности лечения ингибиторами CDK4/6 у пациенток с HR+HER2-метастатическим раком молочной железы. Онкология. Журнал им. П.А. Герцена. 2023;12(3):34-41. doi: 10.17116/onkolog20231203134.
71. Иванова М.И., Матякин Г.Г., Иванов В.М., и др. Роль меглюмина натрия сукцината в профилактике кардиотоксичности, индуцированной химиолучевой терапией у больных раком молочной железы. Онкология. Журнал им. П.А. Герцена. 2023;12(3):42-47. doi: 10.17116/onkolog20231203142.
72. Жерко И.Ю., Демешко П.Д., Науменко Л.В., Красный С.А. Отдаленные результаты применения локальной терапии метастазов меланомы хориоидеи в печени. Онкология. Журнал им. П.А. Герцена. 2023;12(2):5-10. doi: 10.17116/onkolog2023120215.
73. Босиева А.Р., Зикиряходжаев А.Д., Сарибекян Э.К., и др. Возможность выполнения органосохраняющего хирургического лечения у больных раком молочной железы IIB, IIIA, IIIC стадий после неоадъювантной полихимиотерапии. Онкология. Журнал им. П.А. Герцена. 2022;11(6):12-17. doi: 10.17116/onkolog20221106112.
74. Вологирова М.А., Волченко Н.Н., Дрошнева И.В., Сидоров Д.В. Роль некоторых клинико-морфологических факторов в оценке эффективности неоадъювантного химиолучевого лечения аденокарциномы прямой кишки. Онкология. Журнал им. П.А. Герцена. 2022;11(6):26-30. doi: 10.17116/onkolog20221106126.
75. Куликов Е.П., Судаков А.И., Каминский Ю.Д., и др. Электромиография в оценке функциональных результатов комбинированного лечения рака прямой кишки. Онкология. Журнал им. П.А. Герцена. 2022;11(5):19-24. doi: 10.17116/onkolog20221105119.
76. Багдасарова Д.В., Зикиряходжаев А.Д., Усов Ф.Н., и др. Факторы прогноза у больных первично-операбельным раком молочной железы (cT1-2N0-1M0) после реконструктивно-пластических операций с одномоментной реконструкцией эндопротезом. Онкология. Журнал им. П.А. Герцена. 2022;11(4):34-38. doi: 10.17116/onkolog20221104134.
77. Амосова В.А., Петровский А.В., Трофимова О.П., и др. Отдаленные результаты лечения больных раком молочной железы с отеком кожи и неполным ответом на неоадъювантную лекарственную терапию. Онкология. Журнал им. П.А. Герцена. 2022;11(4):39-45. doi: 10.17116/onkolog20221104139.
78. Гамаюнов С.В., Шегурова М.М., Овчинникова Е.Г., и др. Опыт применения атезолизумаба в комбинированной терапии мелкоклеточного рака легкого: анализ собственных данных. Онкология. Журнал им. П.А. Герцена. 2022;11(3):36-40. doi: 10.17116/onkolog20221103136.
79. Ивашина С.В., Бабаева Н.А., Моцкобили Т.А., и др. Атрофия или гиперплазия эндометрия? Тактика ведения пациенток на фоне антиэстрогенной терапии. Онкология. Журнал им. П.А. Герцена. 2022;11(2):13-19. doi: 10.17116/onkolog20221102113.
80. Манихас Г.М., Луфт В.М., Древаль Р.О., и др. Влияние лечебного энтерального питания на качество жизни онкологических больных, нуждающихся в паллиативной помощи. Онкология. Журнал им. П.А. Герцена. 2022;11(2):33-39.doi: 10.17116/onkolog20221102133.
81. Зикиряходжаев А.Д., Босиева А.Р., Багдасарова Д.В., и др. Полный патоморфологический ответ после неоадъювантной полихимиотерапии у больных раком молочной железы. Онкология. Журнал им. П.А. Герцена. 2022;11(1):23-27. doi: 10.17116/onkolog20221101123.
82. Забережный И.А., Попов М.И., Строяковский Д.Л., Кононец П.В. Влияние сроков предоперационной таргетной терапии на продолжительность жизни пациентов с удаленным первичным очагом немелкоклеточного рака легкого III и IV стадии при наличии мутаций в гене EGFR. Онкология. Журнал им. П.А. Герцена. 2022;11(1):28-33. doi: 10.17116/onkolog20221101128.
83. Лядова М.А., Федоринов Д.С., Лядов В.К., и др. Эффективность и безопасность иммунотерапии у пациентов с опухолями желудочно-кишечного тракта. Поволжский онкологический вестник. 2023;14(4):37-48. doi: 10.32000/20781466-2023-4-37-48.
84. Султанбаев А.В., Измайлов А.А., Липатов О.Н., и др. Региональный опыт применения дурвалумаба в лечении немелкоклеточного рака легкого после радикальной химиолучевой терапии. Поволжский онкологический вестник. 2023;14(2):41-46. doi: 10.32000/2078-1466-2023-241-46.
85. Журман В.Н. Иммунные клетки микроокружения рака яичников. Поволжский онкологический вестник. 2023;14(2):30-40. doi: 10.32000/20781466-2023-2-30-40.
86. Андросова А.А., Орлова Р.В., Гордиев М.Г., и др. Определение патогенных соматических мутаций в структуре нейроэндокринных опухолей желудочно-кишечного тракта. Поволжский онкологический вестник. 2023;14(1):2937. doi: 10.32000/2078-1466-2023-1-29-37.
87. Журман В.Н. Влияние молекулярно-генетических характеристик на прогноз впервые выявленного серозного рака яичников highgrade III-IV стадии в зависимости от вариантов лечения. Поволжский онкологический вестник. 2022;13(4):17-24. doi: 10.32000/2078-1466-2022-4-17-24.
88. Гордеев С.С., Магаррамова З.Н., Мышляков В.С, и др. Редкие злокачественные новообразования в практике онкопроктолога: ретроспективный анализ опыта клиники за 20 лет. Поволжский онкологический вестник. 2022;13(4):31-37. doi: 10.32000/20781466-2022-4-31-37.
89. Батов С.В, Напольских В.М., Чураков И.В. Колоректальный рак в Республике Удмуртия в XXI веке (динамика некоторых статистических показателей). Поволжский онкологический вестник. 2022;13(4):38-44. doi: 10.32000/2078-1466-2022-4-38-44.
90. Меньшиков К.В., Султанбаев А.В., Мусин Ш.И., и др. Опыт применения тирозинкиназного ингибитора кабозантиниба в Республике Башкортостан. Поволжский онкологический вестник. 2022;13(2):7-20.
91. Рощина К.Е., Москвина Е.А., Гаспарян Т.Г., и др. Общая выживаемость и факторы прогноза у пациентов с метастазами рака почки в головной мозг после нейрохирургического лечения. Поволжский онкологический вестник. 2022;13(2):49-57.
92. Панченко И.С., Родионов В.В., Бурменская О.В., и др. Клинико-морфологические особенности молекулярно-генетических кластеров трижды негативного рака молочной железы. Поволжский онкологический вестник. 2022;13(1):8-17.
93. Ибрагимова М.К., Цыганов М.М., Литвяков Н.В. Полнотранскриптомный анализ опухоли молочной железы в процессе неоадъювантной химиотерапии: связь с ответом на предоперационную химиотерапию. Успехи молекулярной онкологии. 2022;9(1):33-41. doi: 10.17650/2313-805X-2022-9-1-33-41.
94. Яровая В.А., Яровой А.А., Чудакова Л.В., и др. Комплексный анализ прогностической значимости аберраций хромосомы 8 у пациентов с увеальной меланомой. Успехи молекулярной онкологии. 2022;9(1):57-63. doi: 10.17650/2313805X-2022-9-1-57-63.
95. Мазуренко Н.Н., Югай В.В., Цыганова И.В., и др. Молекулярная гетерогенность и анализ отдаленной выживаемости пациентов с гастроинтестинальными стромальными опухолями. Успехи молекулярной онкологии. 2022;9(2):4357. doi: 10.17650/2313805X-2022-9-2-43-57.
96. Цыганов М.М., Цыденова И.А., Маркович В.А., и др. Экспрессионная гетерогенность генов семейства ABC-транспортеров и генов химиочувствительности в опухоли желудка, канцероматозе и метастазах в лимфатические узлы. Успехи молекулярной онкологии. 2022;9(4):78-88. doi: 10.17650/2313-805X-2022-9-4-78-88.
97. Павленко И.А., Повилайтите П.Е., Кацияев В.Ю., и др. Мутации в гене PIK3CA при раке молочной железы с низкой экспрессией белка HER2 / neu. Успехи молекулярной онкологии. 2022;9(4):89-95. doi: 10.17650/2313-805X-2022-9-4-89-95.
98. Оганян К.А., Мусаелян А.А., Лапин С.В., и др. Молекулярные маркеры ответа на периоперационную химиотерапию при местно-распространенном раке желудка. Успехи молекулярной онкологии. 2023;10(1):40-48. doi: 10.17650/2313-805X-202310-1-40-48.
99. Яровая В.А., Левашов И.А., Зарецкий А.Р., и др. Прогностическая тонкоигольная аспирационная биопсия увеальной меланомы: молекулярно-генетические факторы риска развития метастазов. Успехи молекулярной онкологии. 2023;10(3):90-97. doi: 10.17650/2313-805X-2023-10-3-90-97.
100. Чулкова С.В., Шолохова Е.Н., Поддубная И.В., и др. Экспрессия мономорфных HLA-детерминант, трансферринового рецептора 1 (TfR1) при молекулярных подтипах рака молочной железы. Российский биотерапевтический журнал. 2022;21(4):50-61. doi: 10.17650/1726-9784-2022-21-450-61.
101. Толстых Е.Э., Тупицын Н.Н. Ключевые маркеры диагностики минимальной остаточной болезни при множественной миеломе. Российский биотерапевтический журнал. 2022;21(1):42-49. doi: 10.17650/1726-9784-2022-21-1-42-49.
102. Чулкова С.В., Шолохова Е.Н., Поддубная И.В., и др. HLA-мономорфные детерминанты первичной опухоли у больных раком молочной железы. Российский биотерапевтический журнал. 2022;21(2):56-66. doi: 10.17650/1726-9784-2022-21-2-56-66.
103. Пасова И.А., Гривцова Л.Ю., Мушкарина Т.Ю., и др. Возможности применения иммунотропных препаратов тимического происхождения у онкологических больных. Российский биотерапевтический журнал. 2022;21(1):57-63. doi: 10.17650/1726-9784-2022-21-1-57-63.
104. Казаков А.М., Лактионов К.К., Саранцева К.А. Генетический профиль пациентов с немелкоклеточным раком легкого I–IIIA стадий. Российский биотерапевтический журнал. 2023;22(1):42-48. doi: 10.17650/1726-9784-2023-22-142-48.
105. Полатова Д.Ш., Гильдиева М.С., Мадаминов А.Ю., и др. Прогностическая роль белков PD-L1 И P53 при плоскоклеточной карциноме ротоглотки в зависимости от статуса вируса папилломы человека. Злокачественные опухоли. 2023;13(3):11-19. doi: 10.18027/22245057-2023-13-3-11-19.
106. Авдюхин И.Г., Перегородиев И.Н., Калинин А.Е., и др. Периоперационная химиотерапия в режиме FLOT у больных операбельной аденокарциномой желудка и кардиоэзофагеального перехода (I–III тип по классификации SIEWERT). Опыт НМИЦ онкологии им. Н.Н. Блохина. Злокачественные опухоли. 2022;12(4):5-13. doi: 10.18027/2224-5057-2022-12-4-5-13.
107. Гордеев С.С., Загидуллина А.А., Нагуслаева А.А., и др. Эффективность предоперационной лучевой терапии у пациентов с перстневидноклеточным раком прямой кишки: ретроспективное исследование случай-контроль. Злокачественные опухоли. 2022;12(3):5-10. doi: 10.18027/2224-5057-2022-12-3-5-10.
108. Семёнов Н.Н., Далгатов К.Д. Повышенный уровень СА125 (МUC16) при метастатическом раке желудка — мощный фактор негативного прогноза выживаемости. Злокачественные опухоли. 2022;12(1):44-50. doi: 10.18027/2224-5057-202212-1-44-50.
109. Каганов О.И., Козлов А.М., Швец Д.С., Миколенко Н.И. Хирургия рака поджелудочной железы — опыт одного центра. Российский онкологический журнал. 2022;27(4):183189. doi: 10.17816/onco584148.
110. Сарычева М.М., Важенин А.В., Мозерова Е.Я. Оценка эффективности многокомпонентного лечения при прогрессировании первичных низкозлокачественных глиом головного мозга. Собственный опыт. Российский онкологический журнал. 2022;27(4):157-163. doi: 10.1.7816/onco456888.
111. Манихас Г.М., Захаренко А.А., Полежаев Д.А., и др. Рак лёгкого в условиях ВИЧ-инфекции. Российский онкологический журнал. 2022;27(5):207-220. doi: 10.17816/onco126475.
112. Протасова А.Э., Орлова Р.В., Лященко В.А. Анализ социально-демографических и клинико-морфологических особенностей распространенных форм инвазивного рака шейки матки. Онкогинекология. 2022;2:44-51. doi: 10.52313/22278710_2022_2_44.
113. Чулкова С.В., Шолохова Е.Н., Поддубная И.В., и др. Иммунологическая характеристика инвазивного рака шейки матки. Онкогинекология. 2022;3:44-56. doi: 10.52313/22278710_2022_3_44.
114. Краснопольская К.В., Новикова О.В., Исакова К.М., и др. Особенности раннего фолликулои эмбриогенеза у пациенток после консервативного лечения атипической гиперплазии и начального рака эндометрия. Онкогинекология. 2022;3:44-56. doi: 10.52313/22278710_2022_3_69.
115. Сагакянц А.Б., Белякова Л.И., Шевченко А.Н., и др. Особенности локального иммунитета у пациентов с неинвазивно-мышечным раком мочевого пузыря различной степени злокачественности. Южно-Российский онкологический журнал. 2022;3(4):58-66. doi: 10.37748/26869039-2022-3-4-6.
116. Селютина О.Н., Гуськова Н.К., Лысенко И.Б., Коновальчик М.А. Профиль экспрессии иммунофенотипических маркерных молекул на В-лимфоцитах у больных хроническим лимфолейкозом на этапах иммунохимиотерапии. Южно-Российский онкологический журнал. 2022;3(4):49-57. doi: 10.37748/26869039-2022-3-4-5.
117. Льянова А.А., Владимирова Л.Ю., Ульянова Е.П., и др. Динамика изменения экспрессии фактора неоангиогенеза VEGF в биоптатах опухолевой ткани у больных плоскоклеточным раком слизистой оболочки полости рта при проведении терапии цетуксимабом и химиотерапии. Южно-Российский онкологический журнал. 2022;3(4):40-48. doi: 10.37748/2686-9039-2022-3-4-4.
118. Казаков А.М., Лактионов К.К., Саранцева К.А., Гордиев М.Г. Результаты таргетного секвенирования немелкоклеточного рака легкого I-IIIA стадий и их связь с клинико-морфологическими параметрами опухоли. Практическая онкология. 2023;24(3):291-299. doi: 10.31917/2403291.
119. Абдулоева Н.Х., Скрипко О.А., Скрябин М.В., и др. Оценка частоты выявления мутаций в генах BRCA 1/2 методом ПЦР в государственном бюджетном учреждении здравоохранения "Санкт-Петербургский клинический научно-практический центр специализированных видом медицинской помощи (онкологический) им. Н.П. Напалкова. Практическая онкология. 2023;24(3):300-306.doi: 10.31917/2403300.
120. Сунь Х., Неред С.Н., Трякин А.А. и др. Результаты комбинированного лечения резектабельного рака желудка в зависимости от статуса микросателлитной нестабильности. Хирургия и онкология. 2023;13(2):17–26. doi: 10.17650/2686-9594-2023-13-2-17-26.
121. Лукмонов С.Н., Беленькая Я.В., Лебедько М.С. и др. Влияние предоперационного лечения на частоту послеоперационных осложнений при раке верхнеампулярного отдела прямой кишки. Хирургия и онкология. 2023;13(2):46–53. doi: 10.17650/2686-9594-2023-13-2-46-53.
122. Сафин И.Р., Родионова А.Ю., Рукавишников Д.В., и др. Особенности маршрутизации, диагностики и комбинированного лечения патологических переломов длинных трубчатых костей опухолевой этиологии. Саркомы костей, мягких тканей и опухоли кожи. 2023;15(2):38-45. doi: 10.17650/2219-4614-2023-15-2-38-45.
Об авторах
В. Ф. АчикянРоссия
Ачикян Владимир Фердинандович — врач
Санкт-Петербург
А. А. Курылев
Россия
Курылев Алексей Александрович — к. м. н., доцент кафедры клинической фармакологии и доказательной медицины; врач-клинический фармаколог
Санкт-Петербург
А. С. Колбин
Россия
Колбин Алексей Сергеевич — д. м. н., профессор, зав. кафедрой клинической фармакологии и доказательной медицины; профессор кафедры фармакологии медицинского факультета
Санкт-Петербург
Рецензия
Для цитирования:
Ачикян В.Ф., Курылев А.А., Колбин А.С. Исследования реальной клинической практики в онкологии: анализ российских публикаций. Реальная клиническая практика: данные и доказательства. 2024;4(1):45-65. https://doi.org/10.37489/2782-3784-myrwd-50. EDN: DIHPQG
For citation:
Achikyan V.F., Kurylev A.A., Kolbin A.S. Real-world data studies in oncology: analysis of the Russian publications. Real-World Data & Evidence. 2024;4(1):45-65. (In Russ.) https://doi.org/10.37489/2782-3784-myrwd-50. EDN: DIHPQG






























