Перейти к:
Возможности фармакологической тромбопрофилактики в микрохирургии в условиях реальной клинической практики
https://doi.org/10.37489/2782-3784-myrwd-065
EDN: JJYBMV
Аннотация
Введение. Тромбоэмболические осложнения представляют собой широкий спектр патологических процессов и остаются распространённым осложнением большинства хирургических вмешательств и одной из ведущих причин неудач при пересадке свободных лоскутов. Тромбоз в месте анастомоза — это не только наиболее частая причина неудач при микрохирургических операциях, но он также является одним из факторов, приводящих к нарушению циркуляции в свободных лоскутах и как следствие неэффективности проведённого лечения.
Цель данного обзора — обсудить многочисленные пути тромбопрофилактики, которые могут сыграть роль в обеспечении выживаемости лоскута после хорошо выполненной операции.
Материалы и методы. При первичном поиске было найдено порядка 10 тысяч статей, опубликованных с 1980 по сентябрь 2024 года. После ознакомления с заголовками и абстрактами, были исключены статьи, в которых анализируются нефармакологические методы тромбопрофилактики, в которых нет указаний на конкретные лекарственны средства, нет указаний на исходы эксперимента или клинического исследования, а также статьи, опубликованные на других языках или полнотекстовые версии, которых не опубликованы в свободном доступе. Итого в обзоре проанализированы 34 полнотекстовые статьи.
Результаты. В рамках данной статьи рассмотрены лекарственные средства, фармакологическое действие которых направлено на предотвращение образования тромбов или их разрушение (антиагреганты, антикоагулянты, фибринолитики) и лекарственные средства, которые опосредовано через другие механизмы действия могут снижать вероятность образования тромбов в пересаженных лоскутах — декстран, простациклин, оксид азота. Ни в одном из проанализированных исследований нет указаний на то, что использование какой-либо группы лекарственных средств может привести к улучшению прогнозов и достоверно сократить количество периоперационных тромботических осложнений.
Заключение. Необходимы исследования более высокого уровня для изучения клинического применения антитромботических препаратов в микрохирургии; однако, учитывая небольшой процент неудач в современной практике, для достижения достаточной мощности необходимо хорошо спланированное исследование, когда все операции выполняются хирургическими бригадами с релевантным опытом, а пациенты рандомизированно распределятся в группы.
Для цитирования:
Золотухина И.Ю., Касимова А.Р., Потапов А.Н. Возможности фармакологической тромбопрофилактики в микрохирургии в условиях реальной клинической практики. Реальная клиническая практика: данные и доказательства. 2025;5(1):13-24. https://doi.org/10.37489/2782-3784-myrwd-065. EDN: JJYBMV
For citation:
Zolotukhina I.Yu., Kasimova A.R., Potapov A.N. Possibilities of pharmacological thromboprophylaxis in microsurgery in real-world clinical practice. Real-World Data & Evidence. 2025;5(1):13-24. (In Russ.) https://doi.org/10.37489/2782-3784-myrwd-065. EDN: JJYBMV
Введение / Introduction
Первая клинически успешная микрохирургическая пересадка свободного лоскута состоялась в 1972 году. Технические достижения и усовершенствования в микрохирургии за последние двадцать лет привели к высокому уровню успеха при свободной пересадке тканей в самых разных клинических ситуациях. Одновременный прогресс в области хирургического и анестезиологического обеспечения, а также улучшение периоперационного сестринского ухода сыграли важную роль в том, что эта техника стала стандартом лечения при многих патологиях. В настоящее время использование свободных лоскутов представляет собой вариант лечения во многих видах реконструктивной хирургии, и опытные бригады сообщают об очень высоких показателях успеха [1]. Несмотря на хорошо разработанные методы профилактики, основным осложнением свободных лоскутов является тромбоз сосудов, в основном венозной этиологии [2][3] (рис. 1). Это часто требует хирургической ревизии и может привести к декомпенсации кровоснабжения и некрозу лоскута. Как правило, лоскуты, которые пересаживают свободно, имеют в составе сосудистой ножки две вены: либо две комитантные вены, либо одну комитантную вену и одну вену из другой сосудистой сети лоскута. Что после выполнения сосудистых анастомозов позволяет осуществлять венозный отток от всего лоскута.
Тем не менее, даже в самых квалифицированных хирургических бригадах по-прежнему регистрируется определённый процент плохих исходов. Тромбоз в месте анастомоза — это не только наиболее частая причина неудач при микрохирургических операциях, но он также является одним из факторов, приводящих к нарушению циркуляции в свободных лоскутах [4]. Все состояния, приводящие к тромбозу, описанные Вирховым встречаются при операциях со свободными лоскутами. Взаимосвязь между продолжительностью операции и риском венозной тромбоэмболии (ВТЭ), вероятно, является многофакторной. В соответствии с патофизиологическими основами ВТЭ, неподвижность в результате длительных хирургических вмешательств может привести к застою крови, гиперкоагуляции и повреждению эндотелия, вызванному растяжением стенки сосуда, что увеличивает риск развития ВТЭ. Венозный застой и ишемия могут способствовать образованию ТГВ за счёт усиления регуляции Р-селектина и местных протромботических микрочастиц. Состояние гиперкоагуляции, а также воспаление и повреждение эндотелия, возникающие во время операции, могут аналогичным образом инициировать каскад свёртывания крови и увеличить риск образования тромбов.
Все тромбоэмболические осложнения в микрохирургии по времени возникновения можно разделить на три основные группы: ближайшие, ранние и поздние. Ближайшими являются тромбозы, которые возникают в ходе оперативного вмешательства и в первые 2 часа после завершения вмешательства (рис. 1). К ранним осложнениям относятся сосудистые тромбозы, возникающие на 1–3 сутки после операции (рис. 2). Поздние тромбозы регистрируются с 4-х по 10-е сутки после вмешательства (рис. 3).

Рис. 1. Интраоперационный тромбоз венозного анастомоза (фотография с экрана операционного микроскопа) свободного кожно-мышечного переднего латерального лоскута бедра на голень (собственный архив)
Fig. 1. Intraoperative thrombosis of the venous anastomosis (photograph from the screen of an operating microscope) of the free skin-muscle anterior lateral flap of the thigh to the lower leg (own archive)
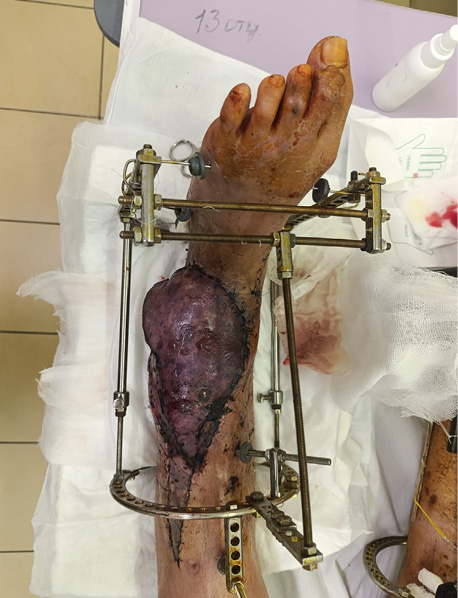
Рис. 2. Тромбоз венозного сосудистого анастомоза свободного пересаженного кожно-мышечного переднего латерального лоскута бедра на голень на 10 сутки после операции, венозный застой лоскута (собственный архив)
Fig. 2. Thrombosis of the venous vascular anastomosis of a free transplanted skin-muscle anterior lateral thigh flap to the lower leg on the 10th day after surgery, venous congestion of the flap (own archive)

Рис. 3. Артериальный тромбоз свободного переднего латерального лоскута бедра, пересаженного на заднюю поверхность голени на 10-е сутки после операции (собственный архив)
Fig. 3. Arterial thrombosis of the free anterior lateral thigh flap transplanted to the posterior surface of the leg on the 10th day after surgery (personal archive)
В случае ближайших и ранних тромбозов в плане спасения лоскута на первый план выходят хирургические методы (ревизия, тромбэктомия с резекцией зоны анастомоза, выполнение новых анастомозов, а в некоторых случаях пластики сосудов аутовенозными вставками) и о применении лекарственных средств можно говорить как о вспомогательной опции — профилактика образования новых тромбов. И наоборот, в случае поздних тромбозов ведущими методами лечения являются консервативные.
К сожалению, фармакологические методы профилактики и лечения тромбозов часто разрабатываются на основе разрозненного опыта лечащих врачей, с заметными различиями в лекарственных средствах, дозировках и сроках применения. Многочисленные исследования на животных и ограниченные проспективные клинические исследования приводят к отсутствию единого мнения о рекомендациях по профилактике и лечению тромботических осложнений. Очевидно, что тромбопрофилактика не может помочь избежать тромбоза при плохом качестве хирургической техники. Однако главная цель рутинной фармакологической тромбопрофилактики — обеспечить безопасность хорошо выполненных пересадок лоскутов. Поскольку вероятность успеха в квалифицированных бригадах достигает 90–98 %, трудно установить определённое преимущество того или иного протокола тромбопрофилактики в показателях эффективности и безопасности.
Цель / Objective данного обзора — это обсудить многочисленные пути тромбопрофилактики, которые могут сыграть роль в обеспечении выживаемости лоскута после хорошо выполненной операции.
Материалы и методы / Materials and methods
Был проведён всесторонний поиск литературы в базах данных PubMed, Scopus, Elibrary по следующим ключевым словам: «free flap» и «microsurgery», а также «thrombosis prevention», «thromboprophylaxis», «anticoagulant», «antiplatelet», «heparin», «low molecular weight heparin», «acetylsalicylic acid», «aspirin», «dextran», «direct oral anticoagulants», «apixaban», «rivaroxaban», «edoxaban», «dabigatran», «fibrinolytic», «Xa factor inhibitors», «thrombin inhibitors», «warfarin». В русскоязычных базах данных поисковый запрос составлялся по такому же алгоритму: «свободный лоскут» и «микрохирургия», а также «профилактика тромбозов», «тромбопрофилактика», «антикоагулянт», «антиагрегант», «гепарин», «низкомолекулярный гепарин», «ацетилсалициловая кислота», «аспирин», «декстран», «прямые оральные антикоагулянты», «апиксабан», «ривароксабан», «эдоксабан», «дабигатран», «фибринолитик», «ингибиторы Xa фактора», «ингибиторы тромбина», «варфарин».
Критериями включения были все статьи, в которых описывается опыт применения лекарственных средств для периоперационной профилактики тромбообразования в пересаженных лоскутов, вне зависимости от их локализации и метода исследования, опубликованные на русском и английском языках. Методология литературного поиска представлена на рис. 4.
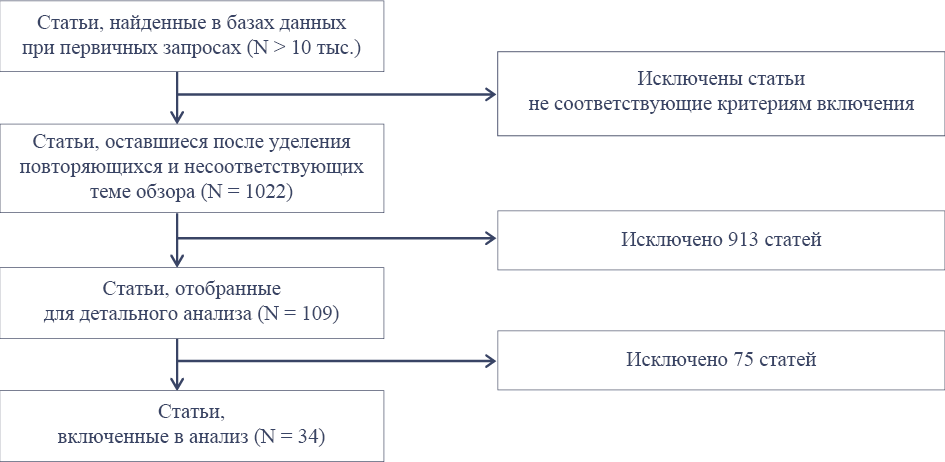
Рис. 4. Методология литературного поиска и отбора исследований
Fig. 4. Methodology of literature search and selection of studies
При первичном поиске было найдено порядка 10 тысяч статей, опубликованных с 1980 по сентябрь 2024 года. Такая глубина поиска была обусловлена с одной стороны уже сформированными техническими возможностями микрохирургических операций, а с другой отсутствием более свежих опубликованных статей, в которых анализируются некоторые группы лекарственных средств. После ознакомления с заголовками и абстрактами, были исключены статьи, в которых анализируются нефармакологические методы тромбопрофилактики, в которых нет указаний на конкретные лекарственные средства, нет указаний на исходы эксперимента или клинического исследования, а также статьи, опубликованные на других языках или полнотекстовые версии, которых не опубликованы в свободном доступе. Итого в обзоре проанализированы 34 полнотекстовые статьи [7–40].
Результаты / Results
В рамках данной статьи рассмотрены лекарственные средства, фармакологическое действие которых направлено на предотвращение образования тромбов или их разрушение (антиагреганты, антикоагулянты, фибринолитики) и лекарственные средства, которые опосредовано через другие механизмы действия могут снижать вероятность образования тромбов в пересаженных лоскутах.
Антиагреганты
Ацетилсалициловая кислота
Механизм действия ацетилсалициловой кислоты (АСК) как антиагреганта заключается в способности в низких дозах селективно ингибировать циклооксигеназу-1, что предотвращает синтез тромбоксана А2, отсутствие которого предотвращает активацию и агрегацию тромбоцитов. При увеличении дозы, селективность действия прекращается и развиваются эффекты связанные и ингибированием циклооксигеназы-2 — снижение синтеза простациклина и угнетение воспалительной реакции [5].
Исследования на животных показали, что АСК предотвращает агрегацию тромбоцитов и образование тромбов в микрососудистых анастомозах [6][7]. Другие исследования не выявили никакого влияния на конечные показатели проходимости [8][9].
Существует большое количество исследований оценивающих влияние АСК на выживаемость лоскутов после свободной их пересадки. В одном из таких исследований в общей сложности было проведено 390 последовательных процедур свободного переноса тканей; 184 пациента не получали послеоперационной тромбопрофилактики, 142 получали АСК, 48 — низкомолекулярный гепарин или комбинацию препаратов, а 16 — инфузию гепарина. Общая частота осложнений составила 38 %, причём в группе, принимавшей АСК, было значительно больше осложнений по сравнению с группой, не принимавшей профилактику (p=0,002). Между приёмом АСК и отсутствием антикоагулянтов не было выявлено существенной разницы в частоте кровотечений (p=0,192) или несостоятельности лоскута (p=0,839). В группе, принимавшей АСК, было проведено больше послеоперационных ревизий (p=0,039). Послеоперационная тромбопрофилактика АСК после свободной пересадки тканей не обеспечивает улучшения выживаемости свободного лоскута и может быть связана с более высокой частотой осложнений [10].
В недавнем метаанализе, обобщающем результаты 14 проведённых исследований, было проведено сравнение использование АСК и других антитромботических лекарственных средств. Не было установлено достоверных отличий между протоколами тромбопрофилактики с применением АСК и использованием других лекарственных средств [11].
Антикоагулянты
Нефракционированный гепарин
Учитывая быстрое начало действия и короткий период полувыведения, подкожное или внутривенное введение гепарина обычно используется в периоперационных условиях. Гепарин усиливает активность антитромбина III, ускоряя его антипротеазную активность и связывание с субстратом в 1 000 раз. Происходит ингибирование каскада свёртывания крови за счёт инактивации факторов свёртывания крови II (тромбина), IX, X, XI и XII [12]. Как правило, интраоперационно используется подкожный болюс в дозе 5000 ЕД, с последующим продолжением применением каждые 8 часов до выписки [13].
Более высокие дозы гепарина, высвобождая оксид азота (NO) из эндотелия сосудов, также приводят к расширению сосудов. Вазодилатация увеличивает скорость кровотока и, согласно триаде Вирхова, также снижает склонность к тромбообразованию [14]. Таким образом, гепарин подавляет образование артериальных и венозных тромбозов и в настоящее время в основном используется для антикоагуляции в микрохирургии. Контроль дозы осуществляется путём измерения активированного частичного тромбопластинового времени (АЧТВ), которое при увеличении в 2 раза по сравнению с нормой указывает на терапевтический эффект гепарина. В исследованиях удалось добиться снижения венозных тромбозов на 60 % путём введения гепарина в терапевтической дозировке.
Частым нежелательным эффектом введения НФГ является значительно повышенная склонность к кровотечениям, в первую очередь в области места наложения анастомоза и из других сосудов лоскута. Риск кровотечения при применении гепарина значительно выше, чем при приёме АСК или декстрана [15]. Другой опасностью гепаринотерапии является гепарин-индуцированная тромбоцитопения (ГИТ I и II). При этом очень редкая форма ГИТ I не модулируется с частотой 1–3 % и возникает только через 5–10 дней после начала введения гепарина, тогда как наиболее распространённая неиммунная форма ГИТ II приводит к падению уровня тромбоцитов <100 х 103 / мкл в течение первых 2 дней после введения гепарина. Согласно данным Segna E. и соавт. ГИТ может быть редкой причиной некроза лоскута и неудачи лечения [16].
Исследования на животных показали, что гепарин может уменьшить образование тромбов и улучшить жизнеспособность лоскута при местном или системном применении [17][18]. Клинические исследования не выявили существенного увеличения частоты возникновения гематом при введении низких доз гепарина в соответствующей дозе для профилактики тромбоэмболии [19, 20]. Ни одно клиническое исследование не продемонстрировало какой-либо пользы от системного применения гепарина для профилактики тромбоза лоскута.
По этим причинам в настоящее время низкомолекулярные гепарины, обладающие большим профилем безопасности рекомендованы к применению.
Низкомолекулярные гепарины (НМГ)
НМГ представляют собой гидролизованный аналог нефракционированного гепарина (НФГ). Они в большей степени ингибируют фактор Ха, но в меньшей степени проявляют антитромбиновую активность (фактор II). Риск возникновения ГИТ II в 10 раз ниже при их использовании. Существует более высокая биодоступность при меньшем неспецифическом связывании и более длительном действии (8–16 ч при абсорбции и 2–3 ч HWZ) [21]. В отличие от НФГ элиминация НМГ происходит почечным путём, поэтому следует упомянуть риск кумуляции при нарушении выделительной функции почек в качестве недостатка по сравнению с НФГ. Поскольку НМГ вызывают лишь небольшое изменение уровня тромбоцитов, корректировка дозы может проводиться на основании измерения анти-Ха активности, в противном случае используются стандартные дозировки согласно инструкции к конкретному лекарственному средству.
НМГ являются стандартной профилактической мерой при венозной тромбоэмболии у пациентов, перенёсших серьёзную операцию, или для тех, кто перенёс более мелкие операции с факторами риска ВТЭ. В исследованиях на животных НМГ показали различные результаты в отношении своей способности предотвращать образование тромбозов в микрососудистых анастомозах, но в клинических исследованиях не было продемонстрировано явной пользы [22][23].
Фондапаринукс
Фондапаринукс — синтетический ингибитор фактора Ха, для парентерального применения обладающий механизмом действия, аналогичным механизму действия гепарина и НМГ [24]. Фондапаринукс не ингибирует активность тромбина, не является ингибитором тканевого фактора высвобождения и не обладает другими свойствами гепарина, такими как противовоспалительный, противовирусный, антиангиогенетический, противоопухолевый и антиметастатический эффекты, хотя высокоаффинно взаимодействует с различными протеазами, ингибиторами протеаз, хемокинами, цитокинами, факторами роста и соответствующие им рецепторы. Низкий уровень антитромбина III в крови также влияет на эффективность фондапаринукса. Он имеет более длительный период полувыведения (17–21 час), чем гепарин или НМГ, и назначается один раз в день [25].
В литературе имеются сообщения об очень ограниченном применении фондапаринукса в микрососудистой хирургии в качестве средства 2-ой линии тромбопрофилактики у пациентов с развившейся гепарин индуцированной тромбоцитопенией [26]. Однако он не одобрен для использования по этому показанию [27].
Прямые оральные антикоагулянты
К прямым оральным антикоагулянтам (ПОАК), доступным в настоящее время в России, относятся: ингибиторы фактора Ха апиксабан, ривароксабан и эдоксабан, а также прямой ингибитор тромбина — дабигатран [28].
Эти лекарственные препараты не являются препаратами 1-ой или 2-ой линии антикоагулянтной терапии для обычных пациентов микрохирургического профиля, но они могут быть применимы при определённых состояниях гиперкоагуляции или у пациентов с сосудистыми и сердечными заболеваниями, которым требуются микрохирургические процедуры. Пациенты, ранее принимавшие ПОАК, обычно прекращают приём этих препаратов и возобновляют их приём в послеоперационном периоде, когда состоялся хирургический гемостаз. Применение данной группы в базовых протоколах тромбопрофилактики требует дальнейшего изучения.
Прямые ингибиторы тромбина
Прямые ингибиторы тромбина действуют путём прямого связывания с тромбином, снижая его активность. В России зарегистрирован для внутривенного введения только бивалирудин. Необходимо провести ещё исследования, чтобы выяснить конкретную роль этого препарата в микрохирургической тромбопрофилактике. Рекомендуется тесное сотрудничество с гематологами, если это необходимо в периоперационном периоде.
Варфарин
Варфарин — это пероральный антикоагулянт, который ингибирует витамин К зависимую эпоксид редуктазу в печени, что впоследствии снижает выработку витамин К-зависимых факторов свёртывания крови (II, V, VII и X) и антикоагулянтов (протеинов С и S) [29]. Варфарин обычно назначают в послеоперационном периоде, так как он обладает выраженным антикоагулянтным действием, но при этом имеет отсроченное начало эффекта. Как правило, он не используется в арсенале для острой периоперационной фазы тромбопрофилактики в микрососудистой хирургии.
Фибринолитики
В отличии от остальных лекарственных средств из группы, угнетающих систему гемостаз, действие фибринолитиков направлено не на предотвращение тромбоза, а на разрушение уже сформированных тромбов. Все фибринолитики по механизму действия делятся на 2 большие группы — непосредственно ферментные препараты, которые разрушают фибрин (фибринолизин (плазмин), трипсин, химотрипсин) и активаторы плазминогена, которые ускоряют образование плазмина.
Опыт применения фибринолитиков в микрохирургии ограничен и в основном все исследования достаточно старые, опубликованные 10 лет назад и ранее. В обзоре, опубликованном Brouwers K. и соавт. [30] были проанализированы 27 опубликованных исследований. Авторы пришли к выводу, что анализ не выявил убедительных доказательств того, что дополнительное применение специфических тромболитиков повышает вероятность успеха процедур по восстановлению проходимости сосудов в пересаженных лоскутах. В большинстве исследований тромболитики использовались как дополнительная опция к хирургической экстракции тромба. Также необходимо помнить, что исходя из механизма действия фибринолитиков, после их применения всегда сохраняется риск реперфузионного поражения нижележащих тканей.
Коллоидные растворы
Это гетерогенные полисахариды разного размера (10–150 кД). В большинстве стран используется гидроксиэтилкрахмал (HES) 6 %. Их антитромботическая функция обусловлена следующими механизмами — усиление эндогенного фибринолиза, а также снижение адгезии тромбоцитов к vWF и активации тромбоцитов [31].
Декстраны
В отличии от АСК декстран угнетает фактор Виллебранда, фактор VII и образование фибрина и увеличивает объём циркулирующей жидкости. Однако по сравнению с АСК, применение декстрана для профилактики тромбоэмболических осложнений, сопровождается большим количеством осложнений, таких как аллергические реакции, отёк лёгких, инфаркт миокарда, пневмония, нефротоксичность, без влияния на эффективность [32].
В исследовании, проведённом Jayaprasad K. и соавт. был выполнен ретроспективный анализ исходов 172 лоскутов. Было проведено сравнение между двумя группами пациентов (по 86 лоскутов в каждой) с использованием декстрана 40 и без него с точки зрения безопасности и эффективности. Статистически значимых различий в частоте тромботических осложнений между группами выявлено не было. Ни у одного из пациентов не развился острый респираторный дистресс-синдром и не потребовалась длительная искусственная вентиляция лёгких. Ни у одного пациента не было анафилактоидных реакций, связанных с применением декстрана. У тридцати восьми пациентов (43,7 %) в группе А и 21 (25,6 %) пациента в группе В развился послеоперационный ателектаз (р=0,01). У шести пациентов в группе А и у пяти пациентов в группе В — послеоперационная пневмония (р=0,93) [33]. Авторы пришли к выводу, что, хотя декстран 40 не привёл к каким-либо значительным неблагоприятным местным или системным осложнениям, он бесполезен в качестве послеоперационного антитромботического средства при реконструкции головы и шеи со свободным переносом тканей.
Ridha и соавт. в 2005 году опубликовали анализ работы пластических хирургов Великобритании, в котором было обнаружено, что 45 % из них регулярно использовали декстран после микрохирургических процедур [34]. Они не обнаружили существенной разницы в показателях успеха между теми, кому назначали декстран, и теми, кому нет. Декстран в значительной степени утратил популярность из-за потенциального риска анафилаксии и отёка лёгких, а также отсутствия доказательной базы в поддержку его применения.
Оксид азота (NO)
Было показано, что расслабляющий фактор эндотелиального происхождения (EDRF), недавно идентифицированный как оксид азота (NO), играет важную роль в тонусе сосудов, агрегации тромбоцитов, нейротрансформации и иммунологическом ответе. NO ингибирует адгезию и активацию тромбоцитов. Поскольку NO является лабильной молекулой, его необходимо вводить ингаляционно или в качестве прекурсора (доноров NO). В двух исследованиях на животных [35, 36] была показана роль доноров NO (моноат спермина, L-аргинин) при местном или системном введении в свободные лоскуты. В этих же исследованиях показано, что ингибиторы NO снижали артериальную проходимость в пересаженном лоскуте на животных моделях. Необходимы дальнейшие исследования, чтобы оценить роль NO в развитии микрососудистых тромбозов. Вероятно позитивное его влияние не столь высоко, однако необходимо иметь в виду негативный эффект от применения ингибиторов NO. Нитропруссид натрия, как известно, способствует высвобождению NO. Однако гипотензивный эффект, связанный с его применением, приводит к значительному снижению кровотока в свободном лоскуте, что отрицательно сказывается на выживаемости лоскута [37].
Стимуляция простациклиновых рецепторов (IP)
Несмотря на то, что IP обладает многими функциями, определёнными в исследованиях на животных моделях, основная клиническая значимость IP заключается в качестве мощного сосудорасширяющего средства: стимуляторы IP используются для лечения тяжёлых и даже опасных для жизни заболеваний, связанных с патологической вазоконстрикцией (например, легочная гипертензия).
Простациклин PGE (1)
Простациклин — это природный простагландин, вырабатываемый интимой кровеносных сосудов. Это самый мощный из известных ингибиторов адгезии тромбоцитов. Эффект на тромбоциты обычно исчезает в течение 30 минут после прекращения инфузии. Поиск литературы не выявил существенных упоминаний о применении PGE (1) с точки зрения тромбопрофилактики в хирургии. Основным применением является ингаляция PGE (1) при лечении лёгочной гипертензии, эффективность и гемодинамические эффекты которой сопоставимы с ингаляционным NO.
Тем не менее, PGE (1) в настоящее время является одним из самых мощных сосудорасширяющих средств. Внутривенное введение простациклина PGE1 используется для снижения не только лёгочного, но и системного сосудистого тонуса. Этот нежелательный эффект может отрицательно сказаться на перфузионном давлении лоскутов при микрохирургии. Сравнение этого негативного эффекта с потенциальным антитромботическим эффектом требует дополнительных исследований при свободных пересадках лоскутов.
В ходе исследований на животных Lee KS и соавт. [38] продемонстрировали превосходство простациклина над АСК, подтверждённое гистологическим анализом. Этот препарат также успешно применялся в двух клинических исследованиях (2 нг/кг/мин или 1200 нг за 2 часа).
Обсуждение / Discussion
Пересадка свободных лоскутов является ключевой процедурой в реконструктивной хирургии. Несмотря на то, что количество успешных операций со свободными лоскутами растёт, в исследованиях сообщается о тромбоэмболических осложнениях как наиболее распространённой причине несостоятельности лоскута. Тромботические явления часто провоцируются некачественным анастомозом микрососудов, сдавлением ножки, инфекцией или несоответствием донорского сосуда. В попытке улучшить приживаемость лоскута различными бригадами в разных странах мира были опробованы многие фармакологические препараты такие, как АСК, гепарин и декстран, и прочие в периоперационном периоде чтобы предотвратить образование тромбов.
Таблица. Основные лекарственные средства, которые потенциально могут использоваться для тромбопрофилактики Table. Main drugs that can potentially be used for thromboprophylaxis | ||||
Лекарственное средство | Группа | Механизм действия | Путь введения | Доза |
Ацетилсалициловая кислота | Антиагрегант | Неселективное необратимое ингибирование ЦОГ-1 и уменьшение агрегации тромбоцитов | п/о | 100 мг |
Декстран | Угнетает фактор Виллебранда, фактор VII, разрушает фибриновые сети и увеличивает внутрисосудистый объём | в/в | 20 мл/ч в течение 120 часов | |
Гепарин | Прямой антикоагулянт | Усиливает активность антитромбина III, что впоследствии приводит к инактивации тромбина и фактора Ха | в/в, п/к | Различается в зависимости от показаний, подбирается по АЧТВ |
Низкомолекулярные гепарины | Механизм действия аналогичен механизму действия гепарина (см. выше), но оказывает меньшее влияние на тромбин и имеет более длительный период полувыведения | п/к | Зависит от конкретного лекарственного средства, дозировка не зависит от АЧТВ | |
Фондапаринукс | Синтетический ингибитор фактора Ха с механизмом действия, сходным с гепарином и низкомолекулярным гепарином | п/к | 7,5 мг (пациенты с массой тела ≥ 50, ≤ 100 кг) один раз в день | |
Лекарственное средство | Группа | Механизм действия | Путь введения | Доза |
Варфарин | Непрямой антикоагулянт | Ингибирует витамин К зависимую эпоксидредуктазу в печени, что впоследствии снижает выработку витамин К-зависимых факторов свёртывания крови (II, V, VII и X) и антикоагулянтов (белков С и S) | п/о | Различные — в зависимости от МНО и показаний |
Апиксабан Ривароксабан Эдоксабан | Прямые ингибиторы Xa фактора | Прямой и обратимый ингибитор фактора Ха в системном кровотоке | п/о | Различные — в зависимости от конкретного используемого ПОАК |
Бивалирудин Дабигатран | Прямые ингибиторы тромбина | Прямое ингибирование тромбина в системном кровотоке | Различается в зависимости от показаний | |
Стрептокиназа Урокиназа Активаторы плазмина | Фибринолитики | Прямое разрушение фибрина в сформированном тромбе | в/в, п/к | Различается в зависимости от показаний |
Примечания: ЦОГ — циклооксигеназа; АЧТВ — активированное частичное тромбопластиновое время; МНО — международное нормализованное отношение; п/о — перорально; в/в — внутривенно; п/к — подкожно. Notes: COX — cyclooxygenase; APTT — activated partial thromboplastin time; INR — international normalized ratio; p/o — orally; i/v — intravenously; s/c — subcutaneously. | ||||
Однако существует ограниченное количество клинических исследований, подтверждающих их использование в качестве профилактических агентов при пересадке свободных лоскутов, и в настоящее время нет единого мнения относительно идеального режима. Нет данных, однозначно подтверждающих использование какого-либо лекарственного средства в качестве периоперационной профилактики.
Современные методы антикоагуляции в микрососудистой хирургии, как было установлено, не отличаются друг от друга по эффективности и профилю нежелательных эффектов. В частности, результаты испытаний АСК, гепарина и декстрана на животных значительно различались по сравнению с проспективными и ретроспективными клиническими исследованиями на людях.
Заключение / Conclusion
Нет клинических данных, высокого уровня доказательности подтверждающих успех рутинного применения лекарственных средств, угнетающих тромбообразование в периоперационном периоде, и, с другой стороны, они могут увеличить риск образования гематомы, что в свою очередь может также негативно сказываться на лоскуте.
Лекарственные средства опосредовано влияющие на процесс тромбообразования также не имеют достаточной доказательной базы, чтобы рутинно рекомендовать их применение в клинической практике. Ввиду специфики проблемы, проведение контролируемых рандомизированных клинических исследований затруднено и существует явная нехватка исследований реальной клинической практики, в которых изучалось бы использование различных схем тромбопрофилактики в микрохирургии с использованием свободного лоскута.
К дизайну такого исследования учитывая нынешнюю низкую частоту тромбозов лоскутов должны предъявляться строгие требования. Это должны быть исследования достаточной мощности, с продуманным дизайном, включёнными пациентами с похожей патологией или механизмом травмы и сходными операциями выполненными достаточно квалифицированными бригадами. Вероятно, такими исследованиями смогут стать исследования реальной клинической практики.
Список литературы
1. López-Arcas JM, Arias J, Del Castillo JL, Burgueño M, Navarro I, Morán MJ, Chamorro M, Martorell V. The fibula osteomyocutaneous flap for mandible reconstruction: a 15-year experience. J Oral Maxillofac Surg. 2010 Oct;68(10):2377-84. doi: 10.1016/j.joms.2009.09.027.
2. Futran ND, Stack BC Jr. Single versus dual venous drainage of the radial forearm free flap. Am J Otolaryngol. 1996 Mar-Apr;17(2):112-7. doi: 10.1016/s0196-0709(96)90006-x.
3. Tran NV, Buchel EW, Convery PA. Microvascular complications of DIEP flaps. Plast Reconstr Surg. 2007 Apr 15;119(5):1397-1405. doi: 10.1097/01.prs.0000256045.71765.96.
4. Khouri RK, Cooley BC, Kunselman AR, Landis JR, Yeramian P, Ingram D, Natarajan N, Benes CO, Wallemark C. A prospective study of microvascular free-flap surgery and outcome. Plast Reconstr Surg. 1998 Sep;102(3):711-21. doi: 10.1097/00006534-199809030-00015.
5. Vane JR, Botting RM. The mechanism of action of aspirin. Thromb Res. 2003 Jun 15;110(5-6):255-8. doi: 10.1016/s0049-3848(03)00379-7.
6. Peter FW, Franken RJ, Wang WZ, Anderson GL, Schuschke DA, O'Shaughnessy MM, Banis JC, Steinau HU, Barker JH. Effect of low dose aspirin on thrombus formation at arterial and venous microanastomoses and on the tissue microcirculation. Plast Reconstr Surg. 1997 Apr;99(4):1112-21. doi: 10.1097/00006534-199704000-00030.
7. Cooley BC, Ruas EJ, Wilgis EF. Scanning electron microscopy of crush/avulsion arterial trauma:effect of heparin and aspirin administration. Microsurgery. 1987;8(1):11-6. doi: 10.1002/micr.1920080105.
8. Buckley RC, Davidson SF, Das SK. The role of various antithrombotic agents in microvascular surgery. Br J Plast Surg. 1994 Jan;47(1):20-3. doi: 10.1016/0007-1226(94)90112-0.
9. Basile AP, Fiala TG, Yaremchuk MJ, May JW Jr. The antithrombotic effects of ticlopidine and aspirin in a microvascular thrombogenic model. Plastic and Reconstructive Surgery. 1995 Jun;95(7):1258-1264. DOI: 10.1097/00006534-199506000-00018.
10. Lighthall JG, Cain R, Ghanem TA, Wax MK. Effect of postoperative aspirin on outcomes in microvascular free tissue transfer surgery. Otolaryngol Head Neck Surg. 2013 Jan;148(1):40-6. doi: 10.1177/0194599812463320.
11. Khan SA, Tayeb RK. Postoperative outcomes of aspirin in microvascular free tissue transfer surgery-A systematic review and meta-analysis. JPRAS Open. 2023 Nov 10;39:49-59. doi: 10.1016/j.jpra.2023.11.003.
12. Björk I, Lindahl U. Mechanism of the anticoagulant action of heparin. Mol Cell Biochem. 1982 Oct 29;48(3):161-82. doi: 10.1007/BF00421226.
13. Xipoleas G, Levine E, Silver L, Koch RM, Taub PJ. A survey of microvascular protocols for lower-extremity free tissue transfer I: perioperative anticoagulation. Ann Plast Surg. 2007 Sep;59(3):311-5. doi: 10.1097/SAP.0b013e31802fc217.
14. Tangphao O, Chalon S, Moreno HJ Jr, Abiose AK, Blaschke TF, Hoffman BB. Heparin-induced vasodilation in human hand veins. Clin Pharmacol Ther. 1999 Sep;66(3):232-8. doi: 10.1016/S0009-9236(99)70030-5.
15. Pugh CM, Dennis RH 2nd, Massac EA. Evaluation of intraoperative anticoagulants in microvascular free-flap surgery. J Natl Med Assoc. 1996 Oct;88(10):655-7.
16. Segna E, Bolzoni AR, Baserga C, Baj A. Free flap loss caused by heparin-induced thrombocytopenia and thrombosis (HITT): a case report and literature review. ACTA OTORHINOLARYNGOLOGICA ITALICA. 2016;36:527-533; doi: 10.14639/0392-100X-1188
17. Hudson DA, Engelbrecht G, Duminy FJ. Another method to prevent venous thrombosis in microsurgery: an in situ venous catheter. Plast Reconstr Surg. 2000 Mar;105(3):999-1003. doi: 10.1097/00006534-200003000-00024.
18. Savoie FH, Cooley BC, Gould JS. Evaluation of the effect of pharmacologic agents on crush-avulsion arterial injuries: a scanning electron microscopy study. Microsurgery. 1991;12(4):292-300. doi: 10.1002/micr.1920120413.
19. Kroll SS, Miller MJ, Reece GP, Baldwin BJ, Robb GL, Bengtson BP, Phillips MD, Kim D, Schusterman MA. Anticoagulants and hematomas in free flap surgery. Plast Reconstr Surg. 1995 Sep;96(3):643-7. doi: 10.1097/00006534-199509000-00017.
20. Liao EC, Taghinia AH, Nguyen LP, Yueh JH, May JW Jr, Orgill DP. Incidence of hematoma complication with heparin venous thrombosis prophylaxis after TRAM flap breast reconstruction. Plast Reconstr Surg. 2008 Apr;121(4):1101-1107. doi: 10.1097/01.prs.0000302454.43201.83.
21. Hirsh J, Warkentin TE, Shaughnessy SG, Anand SS, Halperin JL, Raschke R, Granger C, Ohman EM, Dalen JE. Heparin and low-molecular-weight heparin: mechanisms of action, pharmacokinetics, dosing, monitoring, efficacy, and safety. Chest. 2001 Jan;119(1 Suppl):64S-94S. doi: 10.1378/chest.119.1_suppl.64s.
22. Yousef MA, Dionigi P. Experimental Thromboprophylaxis with Low Molecular Weight Heparin After Microsurgical Revascularization. J Hand Microsurg. 2015 Dec;7(2):256-60. doi: 10.1007/s12593-015-0196-0.
23. Murthy P, Riesberg MV, Hart S, Bustillo A, Duque CS, Said S, Civantos FJ. Efficacy of perioperative thromboprophylactic agents in the maintenance of anastamotic patency and survival of rat microvascular free groin flaps. Otolaryngol Head Neck Surg. 2003 Sep;129(3):176-82. doi: 10.1016/S0194-5998(03)00603-X.
24. Zhang Y, Zhang M, Tan L, Pan N, Zhang L. The clinical use of Fondaparinux: A synthetic heparin pentasaccharide. Prog Mol Biol Transl Sci. 2019; 163:41-53. doi: 10.1016/bs.pmbts.2019.02.004.
25. PubChem, «Fondaparinux». Просмотрено: 27 января 2025 г. [Онлайн]. Доступно на: https://pubchem.ncbi.nlm.nih.gov/compound/5282448.
26. Mehdizade T, Kelahmetoglu O, Gurkan V, Çetin G, Guneren E. Early Suspicion of Heparin-Induced Thrombocytopenia for Successful Free Flap Salvage: Reports of Two Cases. J Hand Microsurg. 2021 Jul;13(3):178-180. doi: 10.1055/s-0040-1713692.
27. Linkins LA. Heparin induced thrombocytopenia. BMJ. 2015 Jan 8;350:g7566. doi: 10.1136/bmj.g7566.
28. Samama MM. The mechanism of action of rivar-oxaban--an oral, direct Factor Xa inhibitor--compared with other anticoagulants. Thromb Res. 2011 Jun;127(6):497-504. doi: 10.1016/j.throm-res.2010.09.008.
29. Ansell J, Hirsh J, Hylek E, Jacobson A, Crowther M, Palareti G. Pharmacology and management of the vitamin K antagonists: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines (8th Edition). Chest. 2008 Jun;133(6 Suppl):160S-198S. doi: 10.1378/chest.08-0670.
30. Brouwers K, Kruit AS, Hummelink S, Ulrich DJO. Management of free flap salvage using thrombolytic drugs: A systematic review. J Plast Reconstr Aesthet Surg. 2020 Oct;73(10):1806-1814. doi: 10.1016/j.bjps.2020.05.057.
31. Conrad MH, Adams WP Jr. Pharmacologic optimization of microsurgery in the new millennium. Plast Reconstr Surg. 2001 Dec;108(7):2088-96; quiz 2097. doi: 10.1097/00006534-200112000-00041.
32. Disa JJ, Polvora VP, Pusic AL, Singh B, Cordeiro PG. Dextran-related complications in head and neck microsurgery: do the benefits outweigh the risks? A prospective randomized analysis. Plast Reconstr Surg. 2003 Nov;112(6):1534-9. doi: 10.1097/01.PRS.0000083378.58757.54.
33. Jayaprasad K, Mathew J, Thankappan K, Sharma M, Duraisamy S, Rajan S, Paul J, Iyer S. Safety and efficacy of low molecular weight dextran (dextran 40) in head and neck free flap reconstruction. J Reconstr Microsurg. 2013 Sep;29(7): 443-8. doi: 10.1055/s-0033-1343950.
34. Ridha H, Jallali N, Butler PE. The use of dextran post free tissue transfer. J Plast Reconstr Aesthet Surg. 2006;59(9):951-4. doi: 10.1016/j.bjps.2005.12.031.
35. Chiang S, Azizzadeh B, Buga G, Ignarro L, Calcaterra T, Blackwell K. Local administration of nitric oxide donor significantly impacts microvascular thrombosis. Laryngoscope. 2003 Mar;113(3):406-9. doi: 10.1097/00005537-200303000-00003.
36. Azizzadeh B, Buga GM, Berke GS, Larian B, Ignarro LJ, Blackwell KE. Inhibitors of nitric oxide promote microvascular thrombosis. Arch Facial Plast Surg. 2003 Jan-Feb;5(1):31-5. doi: 10.1001/archfaci.5.1.31.
37. Banic A, Krejci V, Erni D, Wheatley AM, Sigurdsson GH. Effects of sodium nitroprusside and phenylephrine on blood flow in free musculocutaneous flaps during general anesthesia. Anesthesiology. 1999 Jan;90(1):147-55. doi: 10.1097/00000542-199901000-00020.
38. Lee KS, Suh JD, Han SB, Yoo JC, Lee SJ, Cho SJ. The effect of aspirin and prostaglandin E(1) on the patency of microvascular anastomosis in the rats. Hand Surg. 2001 Dec;6(2):177-85. doi: 10.1142/s0218810401000643.
Об авторах
И. Ю. ЗолотухинаРоссия
Золотухина Инна Юрьевна — врач-травматолог-ортопед травматолого-ортопедического отделения № 13
Санкт-Петербург
Конфликт интересов:
Авторы декларируют отсутствие конфликта интересов.
А. Р. Касимова
Россия
Касимова Алина Рашидовна — врач — клинический фармаколог отделения клинической фармакологии; к. м. н., доцент, доцент кафедры клинической фармакологии и доказательной медицины
Санкт-Петербург
Конфликт интересов:
Авторы декларируют отсутствие конфликта интересов.
А. Н. Потапов
Россия
Потапов Александр Николаевич — ординатор
Санкт-Петербург
Конфликт интересов:
Авторы декларируют отсутствие конфликта интересов.
Рецензия
Для цитирования:
Золотухина И.Ю., Касимова А.Р., Потапов А.Н. Возможности фармакологической тромбопрофилактики в микрохирургии в условиях реальной клинической практики. Реальная клиническая практика: данные и доказательства. 2025;5(1):13-24. https://doi.org/10.37489/2782-3784-myrwd-065. EDN: JJYBMV
For citation:
Zolotukhina I.Yu., Kasimova A.R., Potapov A.N. Possibilities of pharmacological thromboprophylaxis in microsurgery in real-world clinical practice. Real-World Data & Evidence. 2025;5(1):13-24. (In Russ.) https://doi.org/10.37489/2782-3784-myrwd-065. EDN: JJYBMV






























