АКТУАЛЬНЫЕ ОБЗОРЫ
В статье исследуется проблема преодоления «долины смерти» в медицинских научно-исследовательских и опытно-конструкторских работах (НИОКР) — критического этапа, на котором многие перспективные проекты не доходят до внедрения и коммерциализации. Выявлены ключевые барьеры, затрудняющие трансляцию научных достижений в практическое здравоохранение, в числе которых организационно-правовые, финансово-экономические и научно-методические. Особое внимание уделено анализу законодательной базы, регулирующей научную деятельность в России, а также оценке социально-экономического эффекта от внедрения новых медицинских технологий на основе международного опыта. Подчёркивается парадокс: несмотря на значительные инвестиции в медицинские НИОКР, многие проекты терпят неудачу из-за сложностей оценки инновационного потенциала, недостаточной координации между участниками процесса и жёстких регуляторных требований. Предложены пути решения проблемы, включая развитие государственно-частного партнёрства, оптимизацию регуляторных процессов, развитие трансляционной медицины и внедрение систем управления знаниями. Статья адресована исследователям, регуляторным органам, представителям фармацевтических компаний и организаторам здравоохранения, заинтересованным в ускорении внедрения медицинских инноваций.
БЕЗОПАСНОСТЬ ЛЕКАРСТВ
Введение. Высокотехнологичные лекарственные препараты (ВТЛП) удовлетворяют важные медицинские потребности, но требуют особых условий хранения и транспортировки. В связи с этим управление рисками, возникающими на логистических цепочках поставок для них чрезвычайно актуально. Транспортировка в таких случаях происходит в виде замороженных или незамороженных клеток. Криоконсервация является золотым стандартом хранения и транспортировки живых клеток, но её влияние на обеспечение поддержания качества лекарственных препаратов (ЛП) до сих пор не до конца изучено. При транспортировке замороженных клеток некоторые вопросы безопасности решаются строго в индивидуальном порядке: материалы, используемые для производства основного контейнера и применяемых криопротекторных реагентов. В связи с этим разработка подходов к управлению логистических рисков для ВТЛП является актуальным для развития рынка ВТЛП в России.
Цель. Разработка критериев для оценки контрагентов и поставщиков услуг на рынке обращения ВТЛП держателями регистрационных удостоверений (ДРУ).
Материалы и методы. Материалами послужили результаты анализа мировых и собственных научных данных и нормативные документы в соответствующей сфере. Применены общенаучные методы, системный и процессный подходы, методы анализа, синтеза, экстраполяции.
Результаты. Проведена оценка рисков, возникающих на логистических цепочках поставок лекарственных препаратов. Обоснованы критерии для выбора поставщика услуг по перевозке ВТЛП и других термолабильных ЛП для ДРУ, применяемые для снижения рисков, связанных с логистическими цепочками. На основании разработанных критериев рекомендуется проводить оценку потенциальных поставщиков услуг по перевозке ЛП. Обоснована разработка рекомендаций по управлению рисками ВТЛП для инвесторов, фармацевтических производителей и дистрибьютеров для локализации производства и реализации ВТЛП.
Выводы. Проведён анализ рисков, возникающих при перевозке, хранении ЛП, требующих особых условий хранения. Выявлено, что управление рисками ЛП на этапе распределения требует комплексного подхода.
Введение. Данная работа является продолжением изучения безопасности лекарственной терапии в клинических исследованиях, в рамках которого был предложен алгоритм принятия решений на основе метода количественного интегрального анализа нежелательных явлений (НЯ). Для внедрения разработанного алгоритма в клиническую практику необходима его апробация на различных группах лекарственных средств. В качестве препарата для тестирования выбраны вакцины для активной профилактики вирусного гепатита А. Полученные результаты могут стать основой для оценки возможностей метода при формировании прогноза развития неблагоприятных реакций в процессе вакцинопрофилактики.
Цель. Определение эффективности и перспективных направлений применения индивидуализированного интегрального анализа нежелательных явлений по результатам клинических испытаний на примере вакцин для активной профилактики вирусного гепатита А.
Материалы и методы. Индивидуализированная интегральная оценка НЯ выполнена с использованием алгоритма, основные этапы которого подробно представлены в предыдущих работах авторов, по результатам клинических исследований безопасности и иммуногенности вакцины против вирусного гепатита А, проведённых в соответствии с регуляторными и этическими требованиями Российской Федерации. На этапе определения весовых коэффициентов был осуществлён экспертный опрос для оценки важности отдельных характеристик НЯ с использованием метода анализа иерархий. Математико-статистический анализ индивидуализированных интегральных оценок проводили с использованием валидированного программного обеспечения. Для решения задачи оценки информативности и дискриминационной значимости гендерно-возрастных и клинико-лабораторных показателей с целью последующего прогноза возможного развития неблагоприятных отклонений в состоянии здоровья использовали модуль GDA — Общие модели дискриминантного анализа.
Результаты. В процессе реализации основных этапов количественного интегрального анализа НЯ по результатам клинического исследования вакцин для профилактики вирусного гепатита А на системно-органном и организменном уровнях получены данные, свидетельствующие об отсутствии необходимости дополнительной экспертной оценки или повторного проведения исследования этого препарата. Установленная в настоящей работе частота встречаемости нежелательных реакций по отдельным органам и системам была выше уровня для аналогичных вакцин, приведённых в протоколе исследования. С использованием дискриминантного анализа проведена оценка информативности от- дельных гендерно-возрастных и клинико-лабораторных показателей, полученных во время скрининга добровольцев, для разделения групп лиц с повышенной и умеренной индивидуальной чувствительностью к введению вакцин для профилактики вирусного гепатита А. Установлено, что только 8 из 37 показателей вносили статистически значимый вклад в разделение анализируемых групп. Изучаемые показатели имели низкую информативность, что свидетельствует о недостаточной специфичности признаков среди данных скринингового обследования для прогноза развития неблагоприятных отклонений в состоянии здоровья. Общий уровень дискриминации анализируемых групп на основе данных скринингового обследования добровольцев составил около 79 %. Доля правильной классификации группы лиц с повышенной индивидуальной чувствительностью к введению препарата составила 63 %.
Выводы. Разработанный и апробированный на примере вакцин для профилактики вирусного гепатита А метод количественного интегрального анализа НЯ показал перспективность его применения для выделения лиц с повышенной индивидуальной чувствительностью в ходе вакцинопрофилактики на основе исходных гендерно-возрастных, демографических и клинико-лабораторных показателей. Дальнейшие исследования планируется проводить на объединенных данных о нежелательных реакциях при применении вакцин со сходными органоспецифическими и системными нарушениями как в ходе клинических исследований, так и по данным автоматизированной информационной системы «Фармаконадзор», а также путём расширения методов математико-статистической обработки данных, включая нейросетевой анализ.
КОГОРТНЫЕ ИССЛЕДОВАНИЯ
Актуальность. Внедрение ингибиторов CDK4/6 (палбоциклиб, рибоциклиб, абемациклиб) в клиническую практику существенно улучшило результаты лечения больных HR+/HER2-метастатическим раком молочной железы (мРМЖ). Однако отсутствие достоверных предикторов ответа на терапию ограничивает возможности персонализации лечения. Лейкопения, как наиболее частое гематологическое осложнение терапии CDK4/6-ингибиторами, может не только отражать степень миелосупрессии, но и служить косвенным индикатором фармакодинамического эффекта, связанного с подавлением пролиферации клеток костного мозга через механизм, аналогичный таргетному действию на опухоль. Несмотря на отдельные исследования, демонстрирующие потенциальную связь между степенью лейкопении и эффективностью терапии, данные реальной клинической практики остаются противоречивыми и недостаточно систематизированными.
Цель. Ретроспективное изучение в исследуемой когорте возможных предикторов эффективности CDk4/6 ингибиторов в условиях реальной клинической практики.
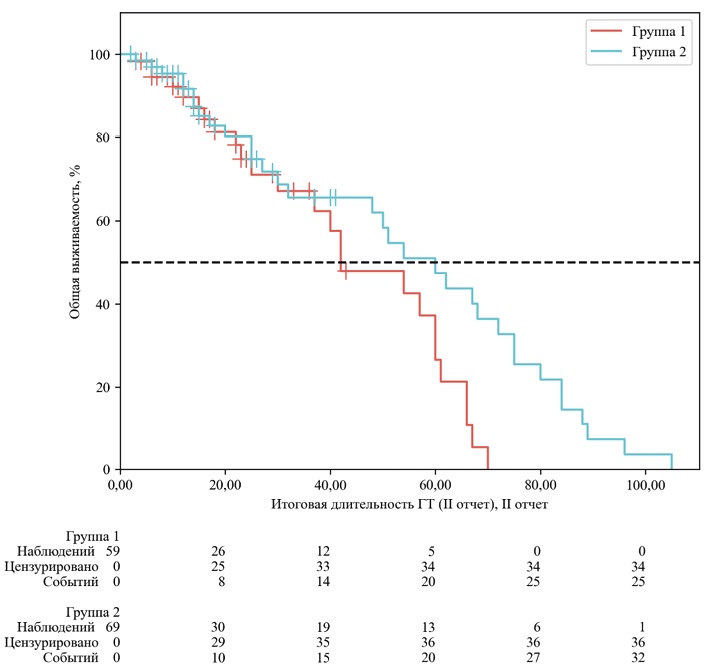
Материалы и методы. Проведён ретроспективный, многоцентровой анализ данных 170 больных HR+/HER2-мРМЖ, получавших терапию ингибиторами CDK4/6 (палбоциклиб или рибоциклиб) с 2019 по 2020 год в пяти онкологических центрах Сибири и Дальнего Востока. Пациентки были стратифицированы на две группы на основании максимальной степени токсичности по CTCAE v5.0: группа 1 (лейкопения G0–1, n=81) и группа 2 (лейкопения G≥2, n=89). Первичной конечной точкой была общая выживаемость (ОВ), вторичной — выживаемость без прогрессирования (ВБП).
Результаты. Пациентки в группе 2 (лейкопения G≥2) продемонстрировали статистически значимое увеличение медианы ОВ по сравнению с группой 1 (лейкопения G0-1): 60,0 месяцев (95 % ДИ: 32,0–72,0) против 42,0 месяцев (95 % ДИ: 30,0–60,0), соответственно (отношение рисков [HR] 0,64; 95 % ДИ: 0,42–0,97; p=0,034). В анализе выживаемости без прогрессирования (ВБП) наблюдалась тенденция к улучшению в группе 2 (медиана 68,0 против 60,0 месяцев), однако она не достигла статистической значимости (p >0,05).
Заключение. В исследовании реальной клинической практики развитие лейкопении 2 степени и выше на фоне терапии ингибиторами CDK4/6 было ассоциировано с улучшением показателя общей выживаемости. Эти данные подтверждают, что степень миелосупрессии может служить ценным и легкодоступным предиктивным биомаркером эффективности лечения.
КАЧЕСТВО ЖИЗНИ
Актуальность. Проблемы третьих моляров оказывают многофакторное негативное воздействие на качество жизни пациентов в современном обществе, затрагивая медицинские, психологические, социальные и экономические аспекты жизнедеятельности. Комплексная оценка данного влияния является актуальной задачей для оптимизации стоматологической помощи и улучшения качества жизни пациентов.
Цель. Провести систематический анализ современных данных о влиянии третьих моляров на различные аспекты качества жизни пациентов с оценкой медицинских, психологических, социальных и экономических факторов воздействия.
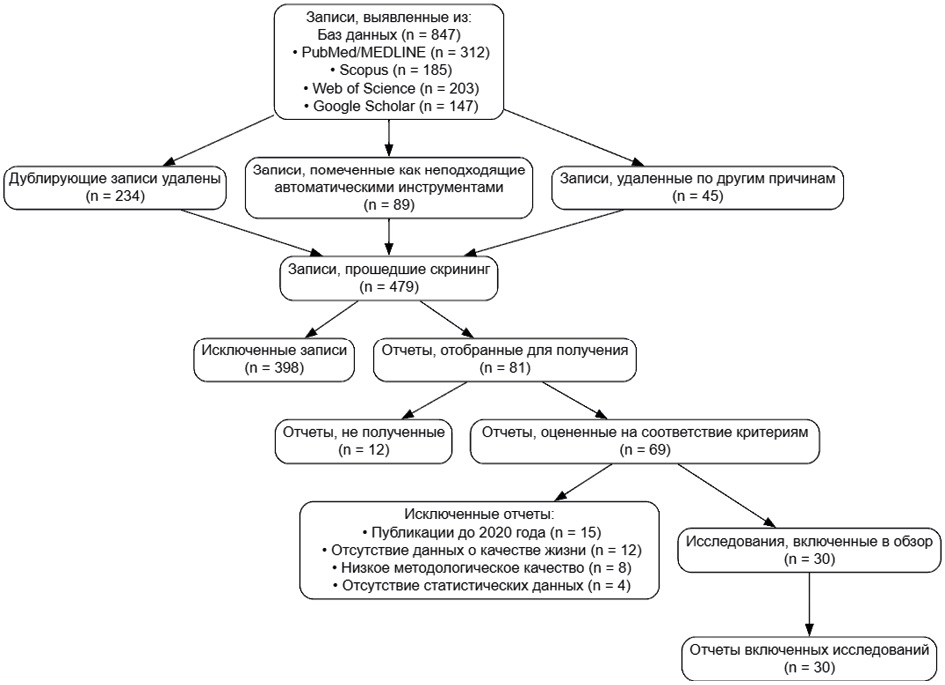
Материалы и методы. Проведён систематический обзор научной литературы в период с 2020 по 2025 года с использованием баз данных PubMed, Scopus, Web of Science и Google Scholar. Критерии включения предусматривали публикации после 2020 года, содержащие статистические данные о влиянии третьих моляров на жизнедеятельность пациентов. Применялся метод контент-анализа для систематизации данных с использованием валидированных инструментов оценки качества жизни, включая OHIP-5, PSQI, AIS и ESS.
Результаты. Установлено, что 52 % пациентов с проблемами третьих моляров страдают от нарушений сна с показателем бессонницы 5,56±3,23 балла по шкале AIS. Риск развития кариеса соседних зубов увеличивается в 1,39 раза, резорбции корней — в 6,51 раза. Общий балл качества жизни пациентов с ретинированными молярами составляет 0–14 баллов против 0–11 в контрольной группе (p <0,05). Экономический анализ показал, что консервативное ведение является наиболее затратным подходом по сравнению с профилактическим удалением. Стратегия сохранения асимптоматичных третьих моляров обеспечивает снижение расходов для национальных систем здравоохранения.
Выводы. Третьи моляры оказывают значительное негативное влияние на качество жизни пациентов через нарушения сна, стоматологические осложнения и психосоциальную дисфункцию. Построенная модель многофакторного воздействия позволяет прогнозировать потребности в различных видах стоматологической помощи и оптимизировать экономические затраты системы здравоохранения на лечение патологий третьих моляров.
РЕЗОЛЮЦИЯ
В статье представлены результаты работы VI ежегодной научно-практической конференции с международным участием «Реальная клиническая практика. Возможное и реальное», посвящённой вопросам использования данных реальной клинической практики (РКП) и доказательств, полученных на их основе (Real-World Data / Real-World Evidence; RWD/RWE), в системе здравоохранения. В ходе мероприятия был проведён всесторонний анализ текущего состояния нормативно-правового регулирования, методологических и практических аспектов применения РКП в Российской Федерации и странах Евразийского экономического союза (ЕАЭС). Выявлены ключевые системные ограничения, включая пробелы в законодательстве, отсутствие унифицированных методик сбора и анализа данных, проблемы интероперабельности информационных систем, а также вопросы конфиденциальности и обработки персональных данных. Сформулирован комплекс конкретных предложений и рекомендаций, направленных на совершенствование нормативной базы, развитие инфраструктуры для работы с РКП, интеграцию таких данных в процессы оценки технологий здравоохранения, разработку клинических рекомендаций и внедрение инновационных моделей лекарственного обеспечения. Особое внимание уделено необходимости гармонизации подходов на уровне ЕАЭС, стандартизации данных и созданию безопасных механизмов доступа к обезличенной медицинской информации для исследователей и разработчиков. Материалы резолюции предназначены для органов законодательной и исполнительной власти, регуляторов, медицинских и научных организаций, а также представителей фармацевтической отрасли и пациентских сообществ.