2025-04-14
24-25 апреля 2025 года в Санкт-Петербурге состоится XII Всероссийская конференция с международным участием «Актуальные вопросы доклинических и клинических исследований лекарственных средств и клинических испытаний медицинских изделий».
 | Формат проведения конференции: очный с онлайн трансляцией. Место проведения конференции: ФГБОУ ВО ПСПбГМУ им. И.П. Павлова Минздрава России, ул. Льва Толстого д. 6-8, корпус №4, 1 этаж, конгресс-центр. Открытие конференции: 24 апреля 2025 года в 09.00 |
2025-04-09
Текущий статус развития правовой основы использования реальной клинической практики в рамках регулирования обращения лекарственных средств
 | 19 сентября 2024 года Ассоциацией специалистов в области оценки технологии здравоохранения, Ассоциацией клинических фармакологов, Санкт-Петербургским подразделением международного общества фармакоэкономических исследований и научного анализа (ISPOR) была организована и проведена V ежегодная научно-практическая конференция с международным участием «Реальная клиническая практика. Возможное и реальное». |
2025-04-09
Обзор новостей RWD / RWE отрасли за март 2025 г.
 | Представляем вам обзор основных новостей по исследованиям RWD / RWE в отрасли за март 2025 г. |
2025-04-06
Приглашаем вас на образовательный вебинар «Данные реальной клинической практики (RWE/RWD) в редких заболеваниях», 18 апреля 2025 года
 | Данные реальной клинической практики (RWD) становятся важным инструментом поддержки решений в здравоохранении. В сфере редких (орфанных) заболеваний, где традиционные методы получения доказательств часто ограничены, именно RWD позволяют объективно оценивать эффективность и безопасность терапии, отслеживать результаты лечения и формировать обоснованные рекомендации для клинической практики и регулирования. |
2025-04-03
Краткий отчет о международной гармонизации стандартов данных реальной клинической практики среди регуляторов медицинских технологий
 | В журнале Pharmacoepidemiology and Drug Safety опубликована статья "Краткий отчет о международной гармонизации стандартов данных реальной клинической практики среди регуляторов медицинских технологий". Международная гармонизация стандартов реальных данных и доказательств (RWD / RWE) является важнейшим направлением работ для лиц принимающих решение. |
2025-04-02
VII Школа молодых учёных и врачей по фармакогенетике, фармакогеномике и персонализированной терапии (21 мая 2025 г.)
 | Дорогие коллеги! Приглашаем Вас и Ваших учеников на нашу традиционную и уже VII Школу молодых учёных и врачей по фармакогенетике, фармакогеномике и персонализированной терапии, которая состоится 21 мая 2025 года в рамках Конгресса "Безопасность фармакотерапии 360 градусов: Noli nocere. |
2025-04-02
Актуальные возможности данных RWD для повышения доступности лекарственных препаратов
 | 19 сентября 2024 года Ассоциацией специалистов в области оценки технологии здравоохранения, Ассоциацией клинических фармакологов, Санкт-Петербургским подразделением международного общества фармакоэкономических исследований и научного анализа (ISPOR) была организована и проведена V ежегодная научно-практическая конференция с международным участием «Реальная клиническая практика. Возможное и реальное». |
2025-04-01
К 2030 году формирование клинических доказательств будет в большей степени основываться на мнение пациентов
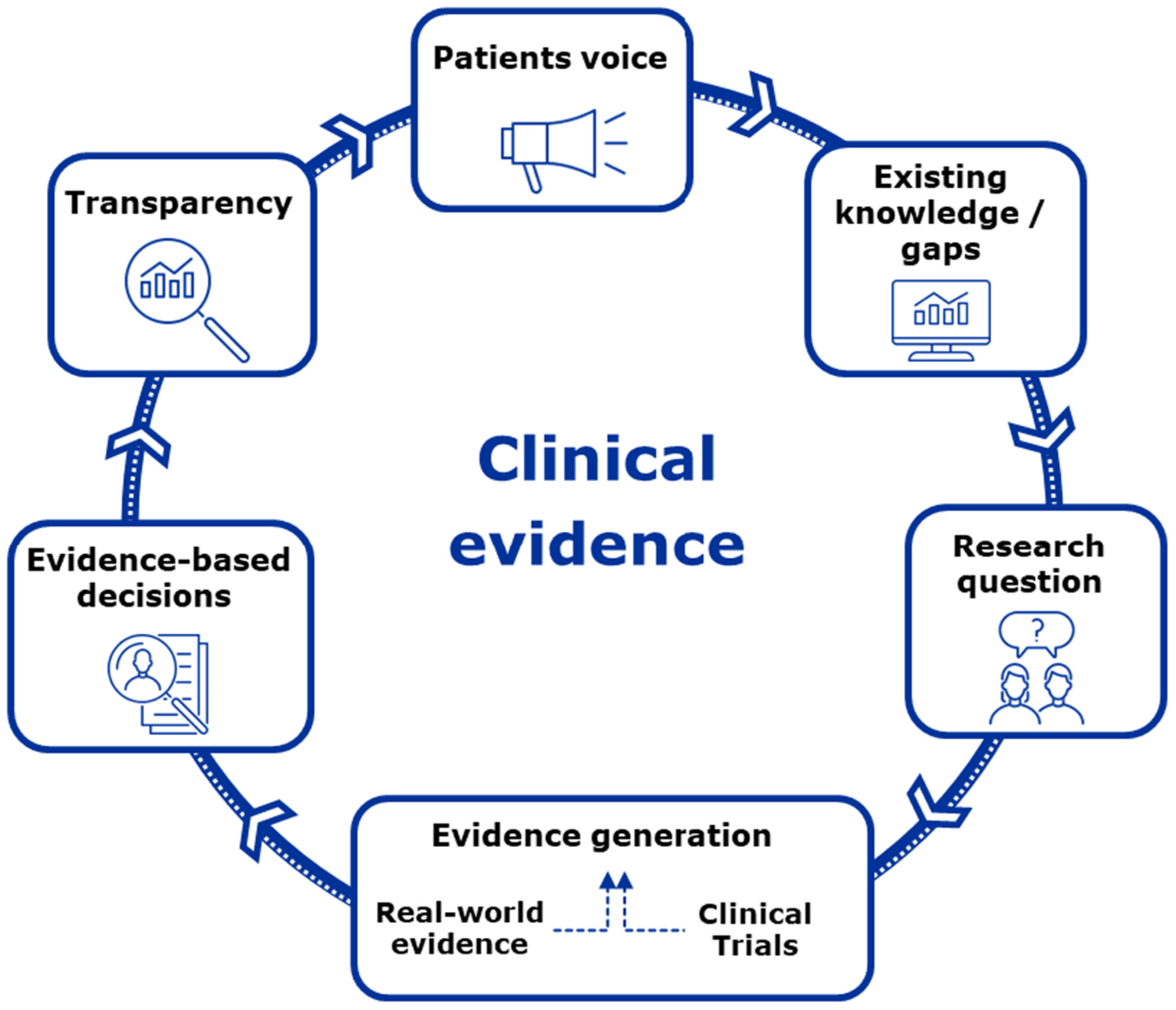 | В журнале Clinical Pharmacology & Therapeutics авторы из European Medicines Regulatory Network (EMRN) рассматривают будущее формирования клинических доказательств (real-world evidence, RWE). |
2025-03-27
Базы данных и регистры в исследованиях реальной клинической практики и фармакоэпидемиологических исследованиях в Северной Америке
 | 19 сентября 2024 года Ассоциацией специалистов в области оценки технологии здравоохранения, Ассоциацией клинических фармакологов, Санкт-Петербургским подразделением международного общества фармакоэкономических исследований и научного анализа (ISPOR) была организована и проведена V ежегодная научно-практическая конференция с международным участием «Реальная клиническая практика. Возможное и реальное». |
2025-03-22
VII Научно-практическая конференция с международным участием «Современные вызовы терапии инфекций»
 | Конференция пройдет в очном формате с частичной трансляцией на портале Medtouch https://medtouch.oragen.ru/calendar/22. Место проведения: Radisson Slavyanskaya, ул. Площадь Евразии, д. 2. Дата мероприятия: 28 марта 2025 г. |
2025-03-19
Пострегистрационные исследования эффективности и безопасности
 | 19 сентября 2024 года Ассоциацией специалистов в области оценки технологии здравоохранения, Ассоциацией клинических фармакологов, Санкт-Петербургским подразделением международного общества фармакоэкономических исследований и научного анализа (ISPOR) была организована и проведена V ежегодная научно-практическая конференция с международным участием «Реальная клиническая практика. Возможное и реальное». |
2025-03-19
Особенности и возможности учета клинических данных по лекарственной терапии в СЗФО. Проблема Персонифицированного учета терапии для повышения качества RWD
 | 19 сентября 2024 года Ассоциацией специалистов в области оценки технологии здравоохранения, Ассоциацией клинических фармакологов, Санкт-Петербургским подразделением международного общества фармакоэкономических исследований и научного анализа (ISPOR) была организована и проведена V ежегодная научно-практическая конференция с международным участием «Реальная клиническая практика. Возможное и реальное». |
2025-03-18
Мировые новости по RWD / RWE за февраль 2025 года.
 | Предлагаем Вам мировые новости по RWD / RWE за февраль 2025 года. |
2025-03-18
I Всероссийская конференция «Клиническая фармакология в педиатрии»
 | В рамках ХХVI Конгресса педиатров России с международным участием «Актуальные проблемы педиатрии», 2 марта 2025 года была проведена I Всероссийская конференция «Клиническая фармакология в педиатрии». I Всероссийская конференция «Клиническая фармакология в педиатрии» состояла из 4 симпозиумов и пленарного заседания. Это была Первая конференция по клинической фармакологии в педиатрии. При этом, ее особенностью стало проведение конференции в рамках Конгресса педиатров России. |
2025-03-12
В Москве прошел V Международный конгресс, посвященный Всемирному дню борьбы с ожирением
 | С 4 по 6 марта 2025 года на базе Московского многопрофильного научно-клинического центра им. С.П. Боткина состоялся V Международный конгресс, посвященный Всемирному дню борьбы с ожирением. Мероприятие собрало ведущих специалистов из разных регионов России и зарубежных стран: эндокринологов, терапевтов, кардиологов, гастроэнтерологов, диетологов, неврологов и врачей смежных специальностей. На протяжении 3 дней продолжалось обсуждение актуальных вопросов диагностики, лечения и профилактики ожирения в клинической практике. |
2025-03-10
Клиническая интерпретация лабораторных исследований в работе врача общей практики
 | Уважаемые коллеги! Приглашаем принять участие в Школе врачей первичного звена «Клиническая интерпретация лабораторных исследований в работе врача общей практики». |
2025-03-09
Эффективность пролголимаба в первой линии у пациентов с метастатической или неоперабельной меланомой кожи с мутацией в гене BRAF в реальной клинической практике
 | 19 сентября 2024 года Ассоциацией специалистов в области оценки технологии здравоохранения, Ассоциацией клинических фармакологов, Санкт-Петербургским подразделением международного общества фармакоэкономических исследований и научного анализа (ISPOR) была организована и проведена V ежегодная научно-практическая конференция с международным участием «Реальная клиническая практика. Возможное и реальное». |
2025-03-07
Использование данных RWD фармакогенетического тестирования для построения моделей прогнозирования возникновения побочных эффектов у пациентов при терапии антипсихотиками
 | 19 сентября 2024 года Ассоциацией специалистов в области оценки технологии здравоохранения, Ассоциацией клинических фармакологов, Санкт-Петербургским подразделением международного общества фармакоэкономических исследований и научного анализа (ISPOR) была организована и проведена V ежегодная научно-практическая конференция с международным участием «Реальная клиническая практика. Возможное и реальное». |
2025-02-25
Медико-экономические эффекты от внедрения RWD и RWE на примере дженериковых лекарственных препаратов
 | 19 сентября 2024 года Ассоциацией специалистов в области оценки технологии здравоохранения, Ассоциацией клинических фармакологов, Санкт-Петербургским подразделением международного общества фармакоэкономических исследований и научного анализа (ISPOR) была организована и проведена V ежегодная научно-практическая конференция с международным участием «Реальная клиническая практика. Возможное и реальное». |
2025-02-23
Значимость RWD для формирования национальной политики в лечении редких заболеваний
 | 19 сентября 2024 года Ассоциацией специалистов в области оценки технологии здравоохранения, Ассоциацией клинических фармакологов, Санкт-Петербургским подразделением международного общества фармакоэкономических исследований и научного анализа (ISPOR) была организована и проведена V ежегодная научно-практическая конференция с международным участием «Реальная клиническая практика. Возможное и реальное». |
2025-02-16
Значение данных реальной клинической практики для лекарственных препаратов, назначаемых вне инструкции по медицинскому применению
 | 19 сентября 2024 года Ассоциацией специалистов в области оценки технологии здравоохранения, Ассоциацией клинических фармакологов, Санкт-Петербургским подразделением международного общества фармакоэкономических исследований и научного анализа (ISPOR) была организована и проведена V ежегодная научно-практическая конференция с международным участием «Реальная клиническая практика. Возможное и реальное». |
--
2025-02-12
Обзор новостей RWD / RWE в мире за январь 2025 года
 | Ознакомьтесь с последними достижениями в области RWD/RWE. |
2025-02-12
В Москве пройдет V Международный Конгресс, посвященный Всемирному дню борьбы с ожирением
 | С 4 по 6 марта 2025 года в Московском многопрофильном научно-клиническом центре им. С.П. Боткина состоится крупнейшее в России мультидисциплинарное научно-практическое мероприятие для врачебного сообщества – V Международный конгресс, посвященный Всемирному дню борьбы с ожирением, призванный объединить специалистов в борьбе с заболеваемостью ожирением. |
2025-02-11
I Всероссийская конференция «Клиническая фармакология в педиатрии», 1 марта 2025 г.
 | В рамках ХХVI Конгресса педиатров России с международным участием «Актуальные проблемы педиатрии», который состоится в Москве в гибридном формате с 28 февраля по 2 марта 2025 года будет проведена I Всероссийская конференция «Клиническая фармакология в педиатрии» (https://congress-pediatr-russia.ru/). |




























